Тепловой эффект реакции – это изменение тепловой энергии, происходящее в результате химической реакции. Он свидетельствует о том, что реакция сопровождается эндотермическим (поглощающим тепло) или экзотермическим (выделяющим тепло) процессом. Знание теплового эффекта реакции играет важную роль в химической кинетике и термодинамике, позволяя предсказывать температурные изменения и направление химических превращений.
Определение теплового эффекта реакции – это процесс измерения или расчета изменения тепловой энергии во время химической реакции. Существует несколько способов определения теплового эффекта реакции: калориметрический метод, использующий калориметры для измерения теплового потока; метод измерения температурных изменений, основанный на измерении изменения температуры среды вокруг реакции; и термохимический метод, основанный на рассчетах, использующих термохимические данные.
Тепловой эффект реакции может быть полезным инструментом для изучения и понимания химических реакций. Он может помочь установить энергетические особенности процессов и определить, какие реакции могут происходить самопроизвольно или требуют энергетической поддержки. Понимание теплового эффекта реакции имеет широкое применение в различных областях, включая химическую промышленность, фармацевтику, энергетику и экологию.
Тепловой эффект реакции
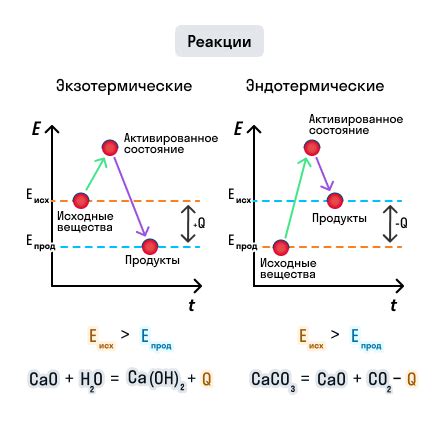
Определение теплового эффекта реакции может быть выполнено с использованием калориметра – устройства, которое позволяет измерять изменение теплоты в процессе химической реакции. Для этого вещества, участвующие в реакции, помещают в калориметр, а затем измеряют изменение температуры системы. По закону сохранения энергии можно определить количество поглощенного или выделенного тепла.
| Тепловой эффект | Значение |
|---|---|
| Эндотермический эффект | Положительное значение |
| Экзотермический эффект | Отрицательное значение |
Тепловой эффект реакции имеет важное значение в химии, так как он позволяет определить энергетическую эффективность реакций и выявить их термодинамические свойства. Эндотермические реакции обычно требуют постоянного поступления тепла, например, в качестве источника энергии для ежедневных процессов жизнедеятельности организмов. А экзотермические реакции могут использоваться в промышленности для получения тепла, освещения и других целей.
Определение и значение
Тепловой эффект реакции является важным показателем, который помогает понять, что происходит во время реакции. Если тепловой эффект реакции положителен (выделяется тепло), это означает, что реакция является экзотермической, то есть происходит выделение энергии в окружающую среду. Если тепловой эффект реакции отрицателен (поглощается тепло), это означает, что реакция является эндотермической, то есть требует поглощения энергии из окружающей среды для своего совершения.
Тепловые изменения во время реакции
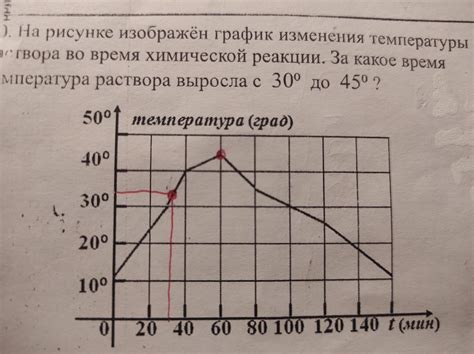
Тепловые изменения во время реакции описываются тепловым эффектом, который представляет собой количество теплоты, выделяющейся или поглощающейся в процессе химической реакции.
Тепловой эффект может быть положительным или отрицательным в зависимости от того, выделяется ли теплота (эндотермическая реакция) или поглощается (экзотермическая реакция). Если тепловой эффект положителен, то это означает, что в процессе реакции выделяется теплота и система становится горячей. Если тепловой эффект отрицателен, то это означает, что в процессе реакции поглощается теплота и система становится холодной.
Тепловой эффект реакции можно определить с помощью калориметра. Калориметр представляет собой устройство, способное измерять количество теплоты, выделяющейся или поглощающейся в процессе реакции.
Измерение теплового эффекта реакции с помощью калориметра включает процедуру, в которой изучаемое вещество добавляется в калориметр, и затем измеряется изменение температуры системы. По изменению температуры и известной теплоемкости калориметра можно определить тепловой эффект реакции.
Тепловые изменения во время реакции играют важную роль в химии. Они не только дают нам информацию о степени реакции и энергии связей, но и могут быть использованы в различных областях, таких как термохимия, энергетика и фармацевтическая промышленность.
Измерение теплового эффекта
Существуют различные методы для измерения теплового эффекта. Один из наиболее распространенных методов - калориметрия. Калориметр - это устройство, способное измерять количество выделяющейся или поглощаемой теплоты во время реакции.
Для измерения теплового эффекта реакции используются калориметры разных типов. Например, калориметры с постоянным давлением (изотермические калориметры) и калориметры с постоянным объемом (адиабатические калориметры).
Процесс измерения теплового эффекта реакции включает следующие шаги:
- Подготовка калориметра и изоляция его от окружающей среды, чтобы минимизировать потерю или проникновение теплоты.
- Произведение реакции внутри калориметра.
- Измерение изменения температуры внутри калориметра с помощью термометра.
- Расчет теплового эффекта реакции с использованием измеренного изменения температуры и характеристик калориметра.
Кроме калориметрии, существуют и другие методы измерения теплового эффекта, такие как термоэлементы и кристаллические методы. Однако, независимо от используемого метода, точность измерения теплового эффекта является основополагающим важным аспектом, поскольку даже небольшие погрешности могут привести к неправильным результатам и неверным выводам.
Тепловой эффект и равновесие

Взаимосвязь теплового эффекта реакции и равновесия определяется принципом Ле-Шателье. Если на систему в состоянии равновесия оказывается внешнее воздействие, изменяющее температуру или концентрацию компонентов, тепловой эффект реакции играет роль компенсатора данного воздействия. То есть, если система пытается снизить свою температуру в результате повышения температуры окружающей среды, она будет выделять тепло путем протекания экзотермической реакции и наоборот.
Попытка изменить концентрации веществ в системе при равновесии приводит к смещению равновесия в ту сторону, где тепловой эффект реакции компенсирует данное изменение концентраций. Это можно объяснить установлением нового равновесия при изменении концентраций, когда система быстро приспосабливается, выделяя или поглощая тепло соответственно в зависимости от характера реакции.
Таким образом, тепловой эффект реакции является важным фактором в определении равновесия химической системы, а также показателем энергетических изменений, происходящих в процессе реакции. Он играет роль компенсатора изменений температуры и концентраций компонентов системы, и его учет позволяет получить более полное понимание химических превращений и их равновесия.








