В атоме каждый электрон движется вокруг ядра, расположенного в его центре. Однако не все электроны занимают одинаковое положение в атоме. Один или несколько электронных слоев, наиболее удаленных от ядра, называют внешними электронными слоями атома.
Завершенный внешний электронный слой атома играет ключевую роль в химических реакциях и связывании атомов с другими атомами. Когда внешний электронный слой полностью заполнен, атом достигает наибольшей устойчивости и имеет малый или нулевой потенциал для участия в химических реакциях.
Значение завершенного внешнего электронного слоя заключается в том, что атомы с таким слоем имеют тенденцию образовывать химические связи с другими атомами, чтобы заполнить свой внешний электронный слой или достичь стабильности. Это приводит к образованию молекул и различных соединений, которые являются основой для разнообразных химических процессов в природе и технологии.
Завершенный внешний электронный слой атома также определяет химические свойства элемента. Например, атомы с одинаковым количеством электронов во внешнем слое обладают подобными свойствами, что позволяет классифицировать элементы в периодической системе Менделеева и предсказывать их химическое поведение.
Понимание значения и смысла завершенного внешнего электронного слоя атома имеет важное значение для различных областей науки и технологии, включая химию, физику, материаловедение и электронику. Изучение внешних электронных слоев позволяет определять свойства различных веществ, находить новые материалы с уникальными свойствами и создавать новые технологии, применяемые в различных отраслях промышленности и медицины.
Внешний электронный слой атома: его структура и функции
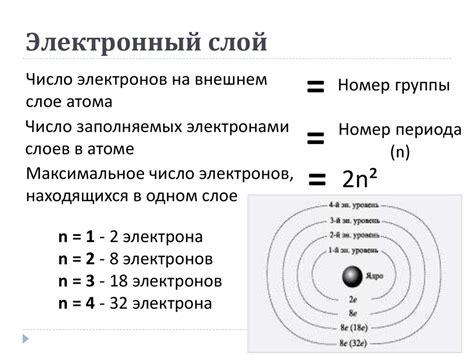
Структура внешнего электронного слоя имеет некоторые особенности. Во-первых, он может содержать до 8 электронов. Это связано с тем, что атомы стремятся достичь стабильной конфигурации, наподобие конфигурации инертных газов, которые имеют полностью заполненный внешний электронный слой.
Функции внешнего электронного слоя весьма важны для химических реакций. Во-первых, электроны в этом слое определяют химическую активность атома. Атомы, имеющие неполный внешний слой (менее 8 электронов), стремятся завершить его, образуя химические связи с другими атомами. Это может происходить путем передачи, получения или обмена электронов.
Вторая функция внешнего электронного слоя связана с формированием молекулярных орбиталей. При образовании молекул электроны двух атомов взаимодействуют, образуя новые орбитали, называемые молекулярными или гибридными орбиталями. Они определяют форму и свойства молекулы и позволяют проводить химические реакции и образовывать новые соединения.
Итак, внешний электронный слой атома имеет важное значение в химии. Его структура и функции определяют химические свойства атомов, и его взаимодействие с другими атомами позволяет образовывать разнообразные химические соединения.
Завершенный электронный слой: понятие и значения
Завершение электронного слоя связано с наличием полностью заполненных и вполне заполняемых подуровней внешней оболочки атома. Обычно это является характерной особенностью инертных элементов, таких как гелий, неон, аргон и другие.
Завершение электронного слоя придает атому особые свойства, так как энергетические уровни на этой оболочке насыщены и не могут принять дополнительных электронов. Это обуславливает столь низкую химическую активность инертных элементов и их способность не образовывать химических связей с другими элементами.
Завершенный электронный слой является ключевым фактором в объяснении химической активности различных элементов и обуславливает их расположение в периодической системе химических элементов.
Таким образом, понятие о завершенном электронном слое атома позволяет объяснить устойчивость и особые свойства некоторых элементов, что имеет важное значение в химии и материаловедении.
Электронная конфигурация и завершенный электронный слой атома
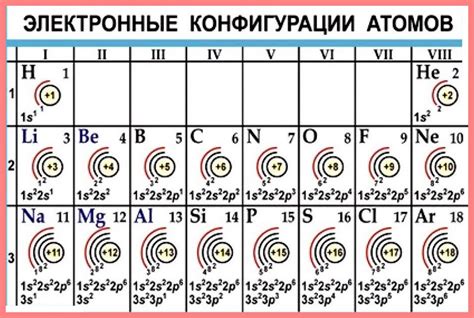
Один из важных концепций в электронной конфигурации - это завершенный электронный слой атома. Завершенный электронный слой атома - это энергетический уровень, на котором электрон удерживается с наибольшей стабильностью и заказанным способом.
Завершенный электронный слой характеризуется тем, что в нем находится максимальное возможное количество электронов для данного уровня энергии. В завершенном слое число электронов равно квадрату номера энергетического уровня. Например, для первого энергетического уровня (n = 1), есть только один электрон. Для второго энергетического уровня (n = 2), есть четыре электрона.
Завершенные электронные слои обладают высокой стабильностью и отвечают за основные химические свойства атома. Атомы стремятся достичь или сохранить завершенные электронные слои, потому что это состояние является энергетически стабильным.
Пример:
Натрий (Na) имеет электронную конфигурацию 1s2 2s2 2p6 3s1. С виду предпоследний энергетический слой 3s1 заполнен одним электроном, поэтому Na стремится потерять его для достижения завершенного электронного слоя. Когда Na потеряет электрон, его электронная конфигурация станет 1s2 2s2 2p6, что соответствует завершенному электронному слою. Поэтому Na образует положительный ион, Na+, чтобы достичь стабильности электронной конфигурации.
Знание электронной конфигурации и завершенного электронного слоя атома помогает понять его химические свойства и реакционную способность. Этот концепт важен для объяснения реакций элементов и связывания атомов в химических соединениях.
Завершенный внешний электронный слой: последствия и свойства
Завершенный внешний электронный слой атома, также известный как "октаэдрический правительство", имеет важные последствия и свойства, которые определяют его роль в химических реакциях и связях.
Последствия завершенного внешнего электронного слоя включают стабильность и инертность атома. Когда внешний электронный слой полностью заполнен, атом не имеет несвязанных электронов, что делает его малоактивным химическим элементом. Атомы с завершенными внешними электронными слоями не стремятся образовывать связи с другими атомами и редко участвуют в химических реакциях. Это объясняет, почему некоторые элементы, такие как гелий или неон, практически не образуют химические соединения.
Свойства атомов с завершенными внешними электронными слоями отражаются в их химической активности и способе образования связей. Атомы с внешними электронными слоями, содержащими от одного до четырех электронов, имеют тенденцию участвовать в химических реакциях, чтобы полностью или частично заполнить свой внешний слой и достичь стабильности. Например, атомы кислорода или селена, имеющие шесть электронов во внешнем слое, стремятся принять два дополнительных электрона, чтобы достичь завершенного внешнего слоя.
Завершенный внешний электронный слой также определяет роль атомов в образовании ионов. Атомы с отсутствием или избытком несвязанных электронов могут вступить в химическую реакцию, передавая или принимая электроны, чтобы достичь стабильных ионных конфигураций. Это позволяет образовывать ионы положительной и отрицательной электрической зарядности и взаимодействовать с другими ионами или молекулами для образования химических соединений.
Таким образом, завершенный внешний электронный слой является ключевым элементом для понимания свойств атомов и их участия в химических реакциях. Он определяет стабильность, инертность и взаимодействие атомов, а также роль элементов в образовании ионов и химических соединений.
Какими электронами заполняется внешний электронный слой?
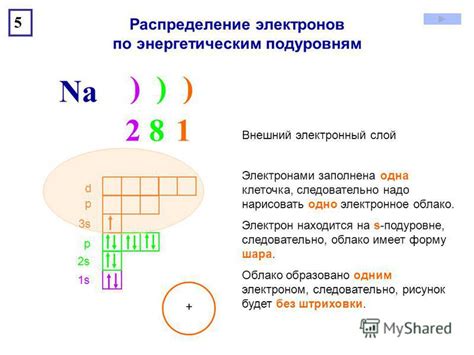
Внешний электронный слой атома заполняется электронами, которые находятся на самом удаленном от ядра уровне энергии. Количество электронов в этом слое определяется порядковым номером элемента в периодической системе Менделеева.
По правилу Маделеева, на внешнем слое может находиться от 1 до 8 электронов. Количество электронов на внешнем слое, также известное как валентная оболочка, определяет химические свойства каждого элемента.
Электроны внешнего слоя называются валентными электронами, и они играют решающую роль в реакциях и взаимодействии атомов. Именно благодаря валентным электронам одни атомы образуют связи с другими, образуя различные химические соединения.
Конфигурация внешнего электронного слоя также определяет химическую активность элемента. Атомы, у которых внешний слой полностью заполнен, обладают низкой химической активностью и зачастую являются инертными газами, такими как гелий или неон. Атомы с неполностью заполненным внешним слоем обладают высокой химической активностью и стремятся завершить свой слой, образуя химические связи с другими атомами.
Роль внешнего электронного слоя в химических реакциях
Внешний электронный слой атома играет важную роль в химических реакциях, определяя его реакционную способность и возможность формирования химических соединений. Электроны во внешнем слое, называемом также валентным слоем, определяют химические свойства атома.
Количество электронов в валентном слое может варьироваться от одного до восьми валентных электронов. Это число определяет способность атома образовывать химические связи и участвовать в химических реакциях. Атомы стремятся заполнить свой внешний электронный слой, приобретая стабильность за счет образования химических связей с другими атомами.
Валентность атома определяет количество электронов, которое он может поделить с другими атомами при образовании химической связи. Например, водородный атом имеет один валентный электрон и может образовывать только одну связь, в то время как кислород имеет шесть валентных электронов и может образовать две связи.
Образование химических связей происходит путем обмена, попарного деления или общего использования валентных электронов. Это позволяет атомам достичь более стабильного энергетического состояния, а также образовывать разнообразные химические соединения.
Внешний электронный слой определяет и химическую активность атомов. Атомы с несколькими валентными электронами имеют большую склонность к реакциям, поскольку они стремятся заполнить или освободить свой внешний слой. Например, атомы с одним валентным электроном, как натрий, часто отдают этот электрон, образуя положительный ион, а атомы с семью валентными электронами, как хлор, часто принимают один электрон, образуя отрицательный ион.
Выводы:
| Роль внешнего электронного слоя в химических реакциях |
|---|
| Определяет реакционную способность атома и возможность формирования химических соединений. |
| Количество валентных электронов в валентном слое определяет способность атома образовывать химические связи и участвовать в химических реакциях. |
| Образование химических связей происходит путем обмена, попарного деления или общего использования валентных электронов. |
| Химическая активность атомов зависит от количества валентных электронов в их внешнем слое. |
Завершенный внешний электронный слой и электроотрицательность
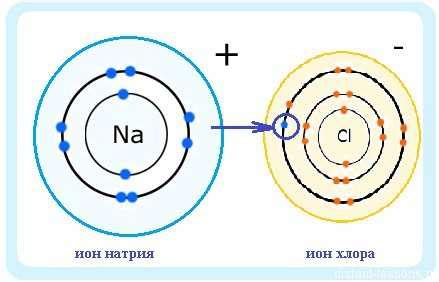
Одним из важных факторов, связанных с завершенным внешним электронным слоем, является электроотрицательность. Электроотрицательность - это способность атома притягивать к себе электроны в химической связи.
Атомы с завершенным внешним электронным слоем обычно имеют низкую электроотрицательность, так как у них уже достаточное количество электронов и нет необходимости притягивать дополнительные. Они являются неподвижными в химических реакциях и обладают высокой химической стабильностью.
С другой стороны, атомы с неполностью заполненным внешним электронным слоем имеют высокую электроотрицательность. Они активно участвуют в химических реакциях и стремятся заполнить свой внешний электронный слой путем притягивания электронов от других атомов. Чем больше необходимо электронов для достижения завершенного внешнего электронного слоя, тем выше электроотрицательность атома.
Значение завершенного внешнего электронного слоя и электроотрицательности заключается в их роли в химических связях и реакциях. Атомы, обладающие завершенным внешним электронным слоем, неизменны и несклонны к реакциям. Электроотрицательные атомы, напротив, обладают большой активностью и могут образовывать химические связи с другими атомами за счет притяжения электронов. В результате этих взаимодействий возникают химические соединения, обладающие различными свойствами.
Завершенный электронный слой атома и его влияние на физические свойства
Когда электронные слои атома полностью заполнены, это означает, что все электроны занимают свои пространственные орбитали вокруг ядра атома. Завершенный электронный слой обычно является наиболее стабильным состоянием атома, и атом стремится сохранить эту стабильность.
Завершенный электронный слой имеет важное влияние на физические свойства атома. Например, атомы с полностью заполненными электронными оболочками имеют более высокую плотность и температуру плавления по сравнению с атомами, у которых электронные слои не полностью заполнены. Это связано с тем, что завершенные электронные слои создают более сильную притяжение между электронами и ядром, что ведет к более компактной структуре атома.
Кроме того, завершенные электронные слои также влияют на химическую активность атома. Атомы с полностью заполненными электронными слоями обычно являются малоактивными и имеют малую способность к образованию химических связей. Это объясняется тем, что в завершенном электронном слое все электроны имеют парный спин и уже находятся в стабильном состоянии. Такие атомы обычно не нуждаются в дополнительных электронах или в отдаче своих электронов для достижения стабильности.
В заключение, завершенный электронный слой атома имеет значительное влияние на его физические свойства, такие как плотность, температура плавления и химическая активность. Атомы с полностью заполненными электронными слоями обычно обладают более высокой плотностью и температурой плавления, а также меньшей химической активностью, по сравнению с атомами, у которых электронные слои не полностью заполнены.








