Строение молекул - это упорядоченная трехмерная архитектура, состоящая из атомов, связанных между собой химическими связями. Каждая молекула имеет свою уникальную структуру, которая определяет ее свойства и функции.
Молекулы играют фундаментальную роль во всех аспектах жизни на Земле. Они образуют все вещества, которые нас окружают - от обычной воды и воздуха до сложных органических соединений, включая белки, углеводы и липиды, составляющие наши органы и ткани. Понимание строения молекул позволяет ученым обобщить и объяснить различные явления и процессы, происходящие в природе.
Система молекулярной биологии и генетики основывается на понимании строения и функции ДНК - двойной спирали, состоящей из молекул нуклеотидов. Эта структура определяет передачу и хранение генетической информации, что является основой для всей жизни на Земле.
Кроме того, изменение строения молекул может привести к изменению их свойств и функций. Например, изменение аминокислотного состава белков может вызвать нарушение их функций и привести к развитию различных заболеваний.
В итоге, изучение строения молекул является основой для понимания физических и химических процессов, происходящих в живых организмах и окружающей среде. Это позволяет разрабатывать новые лекарственные препараты, материалы и технологии, а также предсказывать эффекты различных веществ на наш организм и окружающую среду.
Значение строения молекул
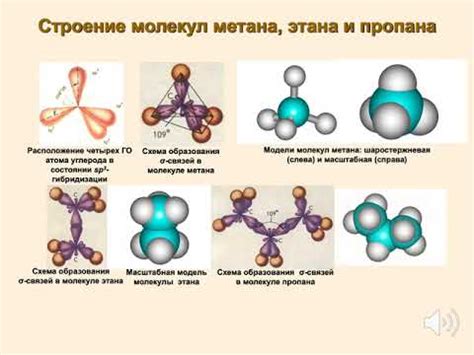
Молекулы представляют собой наименьшие единицы вещества, которые обладают химической активностью. Строение молекул играет важную роль в химических реакциях и определяет их свойства и характер. Молекулы состоят из атомов, которые связаны между собой химическими связями.
Строение молекул определяет их форму, размеры и внутреннюю структуру. Это позволяет молекулам взаимодействовать с другими молекулами и образовывать комплексы, соединения и полимеры.
Молекулярное строение также влияет на физические свойства вещества, такие как плотность, температура плавления и кипения, растворимость. Например, молекулы симметричной структуры могут образовывать кристаллическую решетку, в то время как молекулы несимметричной структуры обычно обладают более низкой степенью упорядоченности.
Кроме того, строение молекул определяет химические свойства вещества. Он оказывает влияние на химическую активность молекулы и способность участвовать в реакциях. Например, формальдегид и этанол имеют одинаковый химический состав, но различное строение - это определяет их различное поведение в реакциях.
Таким образом, строение молекул является важным фактором в понимании химических процессов и связанных с ними свойств вещества. Изучение строения молекул позволяет понять и предсказывать их поведение и использовать эти знания в различных областях, таких как медицина, фармацевтика, материаловедение и энергетика.
Почему строение молекул важно для нас?
Строение молекул определяет их свойства, включая физические, химические и биологические. Физические свойства молекул, такие как температура плавления, плотность и вязкость, могут помочь определить их состояние вещества, а также их поведение под воздействием различных физических условий.
Химические свойства молекул определяют их способность взаимодействовать с другими молекулами и образовывать химические соединения. Эти взаимодействия могут быть как структурными, так и функциональными, и они являются основой для понимания химических реакций и процессов, происходящих в органиках и неорганических системах.
В биологии строение молекул особенно важно, так как оно определяет их функции и взаимодействия внутри клеток и организмов. Знание строения молекул белков, нуклеиновых кислот, углеводов и липидов играет фундаментальную роль в биохимии, молекулярной биологии и генетике. Оно позволяет понять, как клетки выполняют свои функции и как организмы регулируют свои процессы.
Строение молекул также имеет практическое значение. Оно позволяет разрабатывать новые материалы с определенными свойствами, создавать новые лекарственные препараты, проектировать новые энергетические системы и многое другое. Изучение строения молекул и разработка новых технологий на его основе являются ключевыми факторами прогресса и инновации в науке и технологиях.
Как устроены молекулы?

Связи между атомами в молекуле могут быть ковалентными, ионными или металлическими. Ковалентная связь образуется, когда атомы делят пару электронов, что позволяет им образовать устойчивую структуру. Ионная связь возникает между положительно и отрицательно заряженными ионами, которые притягиваются друг к другу. Металлическая связь образуется благодаря перемещению электронов между атомами металла.
Строение молекулы имеет важное значение, так как определяет ее свойства и поведение. Например, вода состоит из молекул, у которых есть полярный характер. Это позволяет им образовывать водородные связи, благодаря чему вода обладает высокой теплоемкостью и способностью к адгезии и сцеплению.
Знание строения молекулы также необходимо для понимания процессов, происходящих в химических реакциях. Взаимодействие молекул зависит от их строения и способности образовывать или разрывать связи. Это позволяет ученым разрабатывать новые материалы, лекарства и прогнозировать результаты реакций.
Роль атомов в молекулах
Молекула образована атомами, которые связаны между собой химическими связями. Атомы, в свою очередь, являются основными строительными блоками вещества, и они играют ключевую роль в формировании структуры молекул.
В молекулах атомы могут соединяться друг с другом различными способами, образуя разнообразные молекулярные структуры. Например, водный молекула состоит из двух атомов водорода и одного атома кислорода, связанных с помощью ковалентных связей.
Различные атомы в молекулах могут обладать разной электроотрицательностью, что влияет на форму и свойства молекулы. Например, наличие атома кислорода в молекуле делает ее полярной и способной образовывать водородные связи.
| Примеры молекул | Состав атомов |
|---|---|
| Вода (H2O) | 2 атома водорода, 1 атом кислорода |
| Аммиак (NH3) | 3 атома водорода, 1 атом азота |
| Метан (CH4) | 1 атом углерода, 4 атома водорода |
Строение молекул и положение атомов в них определяют химические и физические свойства вещества. Например, молекула, состоящая из атомов одного вида, будет иметь другие свойства, чем молекула с различными атомами.
Понимание роли и взаимодействия атомов в молекулах позволяет химикам и ученым разрабатывать новые материалы с определенными свойствами и улучшать существующие вещества для различных применений.
Основные типы молекул в природе

В природе существует огромное количество различных типов молекул, составляющих все живые организмы и все остальные вещества на Земле. Основные типы молекул, которые можно встретить в природе включают:
| Тип молекулы | Описание |
|---|---|
| Вода | Молекула воды, состоящая из одного атома кислорода и двух атомов водорода, является основной составляющей всех живых организмов и играет важную роль во многих химических процессах. |
| Углеводы | Углеводы, такие как глюкоза и сахароза, представляют собой основной источник энергии для организмов. Они состоят из углерода, водорода и кислорода в определенных соотношениях. |
| Белки | Белки являются строительными блоками организма и выполняют широкий спектр функций. Они состоят из аминокислот, соединенных пептидными связями. |
| Липиды | Липиды, такие как жиры и фосфолипиды, играют важную роль в хранении энергии, защите органов и обеспечении структуры клеток. Они состоят из глицерина и жирных кислот. |
| Нуклеиновые кислоты | Нуклеиновые кислоты, включая ДНК и РНК, являются генетическим материалом организмов. Они состоят из нуклеотидов, которые содержат сахар, фосфат и азотистую основу. |
Это только несколько примеров основных типов молекул в природе. Все эти молекулы имеют уникальные свойства, которые определяют их функции и влияют на все химические и биологические процессы в природе.
Взаимодействие молекул в химических реакциях
Химические реакции могут происходить под воздействием различных факторов, таких как тепло, свет, электричество или взаимодействие с другими веществами. В ходе реакции молекулы вступают в контакт друг с другом и происходит обмен электронами или атомами.
Взаимодействие молекул в химических реакциях включает в себя следующие основные типы реакций:
- Синтез (соединительная) реакция. В данном типе реакции две или более молекулы объединяются в новое вещество. Примером может служить реакция образования воды из молекул водорода и кислорода: 2H2 + O2 → 2H2O.
- Анализ (расщепительная) реакция. В этом случае одно вещество разлагается на два или более новых вещества. Примером такой реакции является разложение перекиси водорода: 2H2O2 → 2H2O + O2.
- Замещение (дисплейсерная) реакция. В данном типе реакции атомы или группы атомов одного вещества замещают атомы или группы атомов другого вещества. Примером может служить реакция между хлором и натрием: Cl2 + 2Na → 2NaCl.
- Обратимая (равновесная) реакция. В этом типе реакции происходит обратимое взаимодействие между молекулами, которое может происходить в обоих направлениях. Примером такой реакции является реакция обратимого образования и разложения нитрозильного окиси азота: 2NO2 ⇌ N2O4.
- Окислительно-восстановительная реакция. В данном типе реакции происходит перенос электронов между молекулами, что приводит к изменению степени окисления атомов. Примером может служить реакция между медью и серной кислотой: Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O.
Взаимодействие молекул в химических реакциях позволяет не только образовывать новые вещества, но и изменять их свойства. Благодаря этим процессам возможно синтезирование различных материалов, производство лекарств, создание новых соединений для электроники и других областей науки и промышленности.
Понимание механизма взаимодействия молекул в химических реакциях позволяет ученым предсказывать результаты реакций и разрабатывать эффективные способы синтеза и модификации веществ. Это позволяет добиться значительных прогрессов в различных отраслях науки и технологий.
Связи между атомами в молекулах
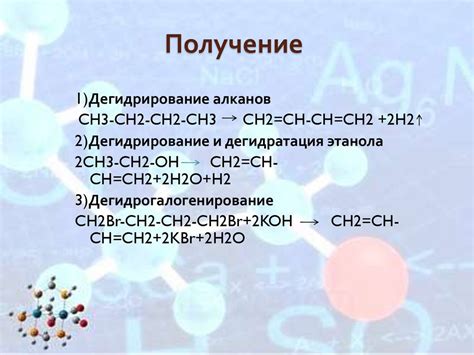
Основными типами химических связей являются ковалентная, ионная и металлическая связи. В ковалентной связи атомы делят электроны, образуя общие электронные пары. В ионной связи атомы образуют ионы с положительным и отрицательным зарядом, которые притягиваются друг к другу. В металлической связи электроны "живут" в общем электронном облаке и перемещаются между атомами.
Связи между атомами в молекулах определяют их физические и химические свойства. Например, длина и прочность химических связей влияют на температуру плавления и кипения вещества, его твердость и прочность. Ковалентные связи обычно более прочные, чем ионные или металлические связи.
Строение молекул и связи между атомами играют важную роль в различных областях науки и технологии. Они определяют свойства и поведение вещества, позволяют создавать новые материалы с нужными свойствами, разрабатывать лекарственные препараты и технологии производства, исследовать и понимать различные биологические процессы и т.д.
Структура полимерных молекул
Основными элементами структуры полимерной молекулы являются мономеры – маленькие молекулы, которые могут повторяться в цепи полимера. Мономеры могут быть однотипными или разнотипными, что влияет на свойства полимера.
Кроме мономеров, полимерные молекулы могут содержать различные функциональные группы, которые придают им определенные свойства и реакционную способность. Эти группы могут быть связаны с основной цепью полимера или находиться на боковых цепочках.
Структура полимерной молекулы определяет множество ее характеристик, таких как механическая прочность, термическая стабильность, электрическая проводимость и другие. Например, наличие разветвлений в структуре полимерной молекулы может повысить ее эластичность и гибкость.
Также структура полимерной молекулы влияет на ее способность взаимодействовать с другими молекулами, что определяет возможные применения полимера. Например, полимеры с определенной структурой могут образовывать сильные связи с поверхностями других материалов, что делает их полезными для создания покрытий и клеевых соединений.
В целом, понимание структуры полимерных молекул является ключевым для разработки новых материалов с желаемыми свойствами и оптимизации существующих материалов для различных приложений в разных отраслях промышленности.
Молекулярная формула и расчет состава вещества

Для определения молекулярной формулы необходимо знать состав вещества. Расчет состава вещества основан на использовании закона сохранения массы и суммарного количества элементов в молекуле.
Расчет состава вещества состоит из следующих шагов:
- Определение суммарной молярной массы всех элементов, входящих в молекулу.
- Расчет молей каждого элемента в молекуле путем деления массы этого элемента на его молярную массу.
- Выражение численных значений соотношений молей в виде простых целых чисел путем деления на меньшее общее значение молей.
- Запись полученных чисел как индексы (маленькие цифры) к символам элементов в молекулярной формуле.
Таким образом, молекулярная формула позволяет узнать точный состав вещества и определить соотношение атомов различных элементов в молекуле. Это важно для понимания свойств и реакций вещества, а также для его использования в различных областях науки и промышленности.
Исследование молекулярного строения с помощью спектроскопии
Одним из методов спектроскопии является инфракрасная спектроскопия. Она используется для изучения колебательных и вращательных движений молекул. Когда инфракрасное излучение проходит через образец, оно взаимодействует с молекулами, вызывая изменение их колебаний. Измерение этих изменений позволяет определить какие-то особенности молекулярной структуры.
Другим методом спектроскопии является ядерное магнитное резонансное исследование (ЯМР). Оно используется для изучения атомных ядер в молекулах. Под действием магнитного поля, атомные ядра выходят из состояния равновесия, что позволяет регистрировать и анализировать их сигналы. ЯМР спектроскопия дает информацию о химическом окружении и взаимодействии атомов в молекуле, что помогает ученым понять ее строение и свойства.
Масс-спектроскопия - это метод, используемый для анализа массы и состава молекул. Он базируется на разделении молекул по их массе и заряду, исследовании их спектров и детектировании частиц. Такой анализ позволяет определить молекулярную массу, состав и структуру образца, что важно для понимания его свойств и функций.
Исследование молекулярного строения с помощью спектроскопии играет важную роль в различных областях науки и технологии. Оно позволяет ученым разрабатывать новые материалы, лекарства и технологии, а также улучшать существующие, обнаруживать аномалии и проблемы, изучать синтез и деятельность биологических систем. Благодаря спектроскопии мы можем получить уникальные сведения о строении и свойствах молекул, что помогает нам лучше понять мир вокруг нас.








