Сильнополярная ковалентная связь - один из важнейших типов химических связей, возникающих между атомами в рамках молекулы. Этот тип связи обладает рядом особенностей, которые влияют на физические и химические свойства вещества.
Суть сильнополярной ковалентной связи заключается в том, что два атома, имеющие недостаток или избыток электронов в внешней оболочке, объединяются путем обмена электронными парами. В результате этого процесса образуется общая область, где оба атома могут поделить пары электронов и сохранить стабильное состояние.
Однако сильнополярная ковалентная связь имеет некоторую специфику, которую следует учитывать. Во-первых, характерная особенность этого типа связи - наличие положительно и отрицательно полярных атомов. При образовании связи между атомами с различными электроотрицательностями, один атом притягивает электроны сильнее, что создает некоторую электрическую разность, или полярность.
Сильнополярная ковалентная связь часто наблюдается между атомами элементов с большой разницей в их электроотрицательности. Например, связь между кислородом и водородом в молекуле воды является типичным примером сильнополярной ковалентной связи.
Значение сильнополярной ковалентной связи
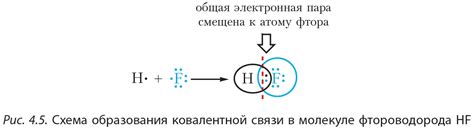
Значение сильнополярной ковалентной связи состоит в стабилизации молекулы и определении ее физических и химических свойств. Разделение зарядов в связи позволяет образовывать дипольные молекулы с моментом диполя. Это способствует образованию внутримолекулярных взаимодействий, таких как водородные связи, которые влияют на свойства соединения, например на кипящую точку и температуру плавления.
Сильнополярные ковалентные связи также играют важную роль в химических реакциях. Полярность связи может влиять на скорость реакции и ее механизм. Вещества, обладающие сильнополярными ковалентными связями, могут быть более химически активными и реакционноспособными, чем вещества с неполярными связями.
Определение и понятие
В сильнополярной связи один атом имеет большую электроотрицательность, чем другой, поэтому он притягивает электроны связи ближе к себе, что приводит к образованию частично заряженных полюсов в молекуле. Такие связи образуются между атомами на противоположных концах электронного неба, поэтому их еще называют диполярными связями.
Сильнополярная ковалентная связь обладает определенными особенностями. Например, в таких связях электронный обмен между атомами является несимметричным, поскольку один атом держит электроны связи ближе к себе. Это приводит к тому, что такие связи обладают полярностью и вызывают образование дипольного момента в молекуле.
Важно отметить, что сильнополярная ковалентная связь является промежуточным типом связи между полностью ионными и неполярными связями. В полностью ионных связях атомы обмениваются электронами, а в неполярных связях электроотрицательность атомов одинакова и электроны связи равномерно распределены между атомами.
Формирование и типы связей
Сильнополярная ковалентная связь формируется между атомами, которые разделяют электроны, но один атом притягивает электроны сильнее, чем другой. Это происходит из-за разницы в электроотрицательности атомов. Атом с более высокой электроотрицательностью образует сильнополярную связь со слабее электроотрицательным атомом.
Основным критерием для определения типа связи является разность в электроотрицательности атомов. Если разность велика (более 1,7 по шкале Полинга), то связь называется ионной. Когда разность находится в диапазоне 0,4-1,7, связь относят к сильнополярным ковалентным связям. Если разность очень мала (менее 0,4), то связь называется неполярной ковалентной связью.
В сильнополярной ковалентной связи электроны, образующие связь, проводят большую часть времени вблизи атома с более высокой электроотрицательностью, что создает разделение зарядов в молекуле. Это приводит к появлению дипольного момента и полярности молекулы.
Тип связи играет важную роль в определении физических и химических свойств вещества. Он влияет на температуру плавления и кипения, растворимость, электропроводность и многие другие свойства вещества.
Особенности сильнополярной связи
Одной из особенностей сильнополярной связи является то, что ее длина и энергия связи варьируются в зависимости от силы притяжения между атомами. Чем сильнее притяжение, тем короче длина связи и выше энергия связи, и наоборот.
Также сильнополярная связь обладает повышенной полярностью по сравнению с другими типами связей, такими как неполярная ковалентная связь или ионная связь. Это связано с тем, что один атом сильнополярной связи притягивает электроны сильнее, создавая неравномерное распределение зарядов в молекуле. Возникающая полярность может вызывать взаимодействия молекул и создавать дополнительные силы притяжения или отталкивания.
Также следует отметить, что сильнополярная связь имеет определенный угол между атомами, что может влиять на конфигурацию молекулы и ее свойства. Угол зависит от типа и характера атомов, формирующих связь.
Важно отметить, что сильнополярная связь играет важную роль в химии органических соединений, биохимии и других областях науки. Понимание ее особенностей позволяет объяснить и предсказать свойства и реакции молекул, а также осуществлять синтез новых соединений с заданными свойствами.
Примеры в природе

Сильнополярная ковалентная связь широко распространена в природе и играет важную роль во многих процессах и явлениях. Ниже приведены некоторые примеры таких связей:
1. Молекулярные соединения: сильнополярные ковалентные связи образуются между атомами различных элементов в молекулах. Например, в молекуле воды (H2O) атом кислорода и два атома водорода образуют сильнополярные ковалентные связи.
2. Белки: белки, основные компоненты живых организмов, состоят из аминокислотных остатков, которые связаны сильнополярными ковалентными связями. Эти связи определяют форму и функцию белков.
3. ДНК: двухцепочечная ДНК, содержащая генетическую информацию, образована сильнополярными ковалентными связями между атомами фосфора и атомами углерода и азота в нуклеотидах.
4. Алмаз: алмаз - одна из форм углерода, в которой атомы углерода образуют сильнополярные ковалентные связи друг с другом. Это делает алмаз одним из самых твердых материалов в природе.
5. Сахар: сахар, такой как сахароза (сахарный песок), состоит из атомов углерода, водорода и кислорода, связанных сильнополярными ковалентными связями. Эти связи определяют структуру и свойства сахара.
Все эти примеры демонстрируют значительное влияние сильнополярной ковалентной связи на различные аспекты жизни и являются наиболее яркими примерами этого типа химической связи в природе.
Значение в химическом процессе
Сильнополярные ковалентные связи играют ключевую роль в химических процессах. Они обладают высокой стабильностью и силой, что позволяет молекулам образовывать устойчивые соединения. За счет сильной электронной привлекательности, сильнополярные связи способствуют образованию комплексных соединений и реакций.
Также сильнополярные связи влияют на физические и химические свойства веществ. Они могут определять плотность, точку кипения, температуру плавления и другие характеристики вещества. Например, вода – это соединение, в котором сильная полярность связи между атомами водорода и кислорода позволяет ей обладать высокой теплоемкостью и способностью образовывать водородные связи.
Сильнополярные связи также могут влиять на химическую активность вещества. Они могут обеспечивать устойчивость молекуле в химической реакции или, наоборот, облегчать ее разрушение. Кроме того, сильнополярные связи могут создавать полюсность молекулы, что обусловливает ее растворимость в различных растворителях.
Важно отметить, что сильнополярные ковалентные связи встречаются в различных химических соединениях, и их наличие и характер могут быть определены с помощью различных методов исследования, таких как спектроскопия и рентгено-структурный анализ.








