Неорганические кислоты — это класс химических соединений, которые обладают кислотными свойствами и состоят из неметалла и водорода или оксигида металла. Они являются одной из важных групп неорганических соединений и применяются в различных областях науки и промышленности.
Неорганические кислоты широко используются в химической промышленности. Например, серная кислота, H2SO4, является одним из ключевых промышленных продуктов. Она используется для производства удобрений, пластмасс, текстильных волокон и других химических продуктов. Фосфорная кислота, H3PO4, также имеет большое промышленное значение и применяется в производстве удобрений, стекла, моющих средств и других продуктов.
Оксиды неорганических кислот также широко применяются в различных отраслях. Например, оксид серы, SO2, используется в производстве азотной кислоты и других органических соединений. Оксид азота, NO2, используется в производстве селитры, азотной кислоты и других продуктов. Оксиды неорганических кислот выполняют важные функции в промышленных процессах, благодаря своим физическим и химическим свойствам.
Неорганические кислоты также имеют широкое применение в научных исследованиях и образовании. Они используются в химическом анализе для определения содержания различных соединений и в создании новых материалов с определенными свойствами. Изучение неорганических кислот помогает углубить понимание основ химии и расширить области их применения.
В заключение, неорганические кислоты представляют собой важный класс химических соединений, которые широко применяются в промышленности, научных исследованиях и образовании. Они обладают разнообразными свойствами и имеют многочисленные области применения. Изучение неорганических кислот позволяет расширить наши знания о химических процессах и создавать новые материалы с новыми свойствами.
Неорганические кислоты: обзор и применение
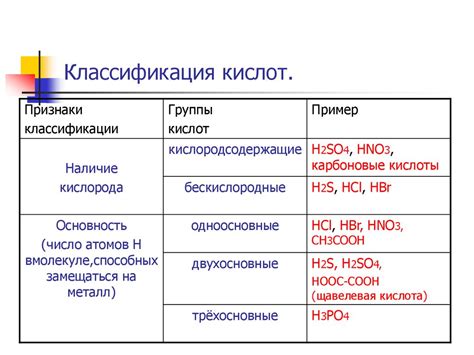
Неорганические кислоты представляют собой вещества, образованные соединением водорода с неорганической основой. Они широко используются в различных областях науки и промышленности.
Одной из наиболее известных неорганических кислот является серная кислота (H2SO4). Она часто применяется в химической промышленности для производства удобрений, пластмасс, бумаги и других продуктов. Серная кислота также используется в лабораториях для проведения различных химических реакций и анализа веществ.
Фосфорная кислота (H3PO4) также довольно распространена. Она является важным компонентом удобрений и используется в производстве пищевых добавок, например, в производстве безалкогольных напитков. Фосфорная кислота также применяется при производстве пластмасс, бытовой химии и других продуктов.
Нитратная кислота (HNO3) находит применение в производстве взрывчатых веществ и удобрений. Она также используется для очистки металлических поверхностей и в лабораторных исследованиях. Нитратная кислота имеет сильное окислительное действие и требует особой осторожности при обращении с ней.
Соляная кислота (HCl) широко используется в промышленности и лабораторной практике. Она используется для очистки металлов, при производстве пищевых продуктов, фармацевтики, текстиля и других отраслях. Соляная кислота также играет важную роль в процессах пищеварения в организмах живых существ.
Неорганические кислоты имеют широкий спектр применения и являются важными компонентами в различных отраслях промышленности и науки.
Что такое неорганические кислоты
Неорганические кислоты могут быть представлены различными элементами, такими как кислород, сера, фосфор, азот и многими другими. Некоторые из наиболее распространенных неорганических кислот включают серную кислоту (H2SO4), соляную кислоту (HCl), азотную кислоту (HNO3) и фосфорную кислоту (H3PO4).
Неорганические кислоты имеют широкое применение в различных областях. Они используются в производстве удобрений, в процессе очистки воды и сточных вод, в металлургии, производстве полимеров, электронике и других отраслях. Они также применяются как химические реагенты в лабораторных исследованиях и анализе веществ.
- Серная кислота (H2SO4) используется в производстве удобрений, в процессе очистки металлов, производстве лекарственных препаратов и других областях.
- Соляная кислота (HCl) применяется в металлургии, производстве пищевых продуктов, очистке воды и других процессах.
- Азотная кислота (HNO3) используется для производства нитроустановок, лекарственных препаратов и других химических соединений.
- Фосфорная кислота (H3PO4) применяется в производстве удобрений, моющих средств, пищевых добавок и других промышленных продуктов.
Неорганические кислоты могут быть также опасны для здоровья и окружающей среды, поэтому требуют специальной обработки и безопасного использования.
Неорганические кислоты являются важными химическими соединениями, которые имеют широкие применения в различных отраслях науки, промышленности и медицины. Изучение и использование неорганических кислот помогает развивать новые технологии и находить решения для многих проблем человечества.
Свойства и состав неорганических кислот
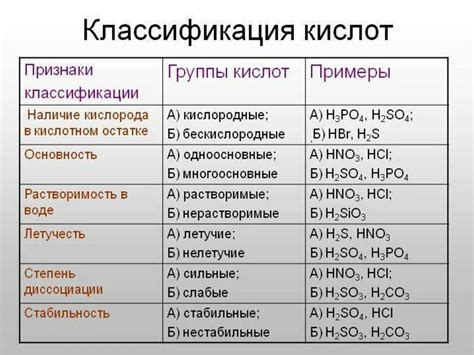
В зависимости от своего состава и структуры, неорганические кислоты могут быть моноосновными, двухосновными или многокислотными. Моноосновные кислоты содержат одну кислотную группу, двухосновные – две, а многокислотные – более двух.
Основные свойства неорганических кислот включают:
- Кислотность – способность отдавать протоны при взаимодействии с другими веществами. Кислотность неорганических кислот зависит от их состава и концентрации. Например, серная кислота (H2SO4) считается одной из самых кислотных неорганических кислот.
- Коррозивность – способность разрушать материалы при взаимодействии с ними. Некоторые неорганические кислоты, такие как соляная кислота (HCl) и азотная кислота (HNO3), являются сильными коррозионно-активными веществами.
- Электролитические свойства – способность разделяться на ионы при растворении в воде. Большинство неорганических кислот являются электролитами и образуют растворы, способные проводить электрический ток.
- Реактивность – способность участвовать в химических реакциях. Неорганические кислоты могут быть использованы для различных видов реакций, таких как нейтрализация, окисление-восстановление и др.
Состав неорганических кислот определяется их химической формулой. Например, серная кислота (H2SO4) состоит из двух атомов водорода, одного атома серы и четырех атомов кислорода. Формула каждой кислоты отражает количество и тип атомов, входящих в ее структуру.
Отличия неорганических кислот от органических
Органические кислоты, в свою очередь, содержат углерод в своей структуре. Они являются производными углеводородов и могут иметь различные функциональные группы, такие как карбоксильные (-COOH) и фенольные (-OH) группы. Например, уксусная кислота (CH3COOH) и лимонная кислота (C6H8O7) являются органическими кислотами.
Одним из основных отличий между неорганическими и органическими кислотами является их происхождение. Неорганические кислоты могут быть получены путем химических реакций, в то время как органические кислоты в основном синтезируются в живых организмах, таких как растения и животные.
Еще одно различие заключается в их химических свойствах. Неорганические кислоты обычно являются сильными кислотами, поскольку они полностью диссоциируют в водном растворе и образуют ионы водорода. Органические кислоты, напротив, могут быть как слабыми, так и сильными кислотами в зависимости от их структуры и функциональных групп.
Важно отметить, что неорганические и органические кислоты имеют различные применения. Неорганические кислоты, например, используются в промышленности для производства удобрений, растворителей и коррозионностойких материалов. Органические кислоты, с другой стороны, широко применяются в пищевой промышленности, фармацевтике и в процессе синтеза органических соединений.
Физические и химические свойства неорганических кислот

Физические свойства неорганических кислот обусловлены их молекулярной структурой и межмолекулярными взаимодействиями. Они могут быть в виде газов, жидкостей или твердых веществ в зависимости от условий температуры и давления.
Химические свойства неорганических кислот определяют их реакционную способность. Кислоты проявляют кислотность при взаимодействии с основаниями, металлами и неорганическими соединениями. Они обладают способностью отдавать протоны (H+) и образовывать соли. Реакции с участием неорганических кислот могут быть взаимодействиями обмена, окисления-восстановления и другими.
Неорганические кислоты обладают различными степенями кислотности, которые характеризуются значениями pH. Некоторые из наиболее распространенных неорганических кислот включают серную кислоту (H2SO4), соляную кислоту (HCl) и азотную кислоту (HNO3). У этих кислот наибольшая кислотность и наибольшее количество протонов, способных отдаваться в реакциях с основаниями и образовывать соли.
Неорганические кислоты в промышленности
Промышленность использует неорганические кислоты в виде различных соединений, таких как серная кислота (H2SO4), соляная кислота (HCl), азотная кислота (HNO3) и фосфорная кислота (H3PO4).
Неорганические кислоты играют важную роль в различных процессах разведения, нейтрализации и очистки веществ. Они используются в производстве удобрений, пластиков, красок и лаков, фармацевтических препаратов, батарей, электроники и многих других областях.
Серная кислота, например, широко применяется в производстве удобрений, в растворителях, а также в процессе очистки металлов. Она также используется в батареях, аккумуляторах и фармацевтике.
Соляная кислота используется в процессе производства хлора и пластиков, а также в очистке металлических поверхностей и процессах гальванизации. Она также играет важную роль в производстве пищевых добавок, железнодорожных сигналов и фармацевтических препаратов.
Азотная кислота находит применение в производстве удобрений, синтезе пластмасс, процессе выработки взрывчатых веществ, а также в производстве красок, красителей и фармацевтических препаратов.
Фосфорная кислота используется в производстве удобрений, моющих средств, красителей, кормов для животных и фармацевтических препаратов.
В целом, неорганические кислоты являются неотъемлемой частью промышленных процессов и находят широкое применение в различных отраслях экономики, обеспечивая эффективные и точные реакции во множестве производственных процессов.
Процесс получения неорганических кислот
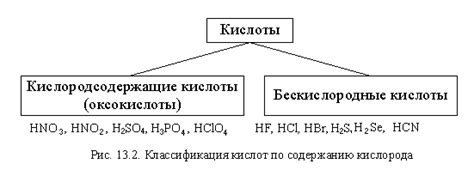
Неорганические кислоты обычно производятся промышленно с использованием различных методов, включая химические реакции и физические процессы. Процесс получения неорганических кислот может варьироваться в зависимости от конкретного вещества и его свойств.
Одним из популярных способов получения неорганических кислот является использование химической реакции. В этом случае, вещество, которое может служить основой для кислоты, соединяется с кислотным агентом. В результате происходит химическая реакция, в результате которой образуется искомая неорганическая кислота.
Другой метод получения неорганических кислот основан на использовании физических процессов. Например, дистилляция может использоваться для получения концентрированных растворов неорганических кислот. В этом случае, раствор кислоты подвергается нагреванию, и затем пары кислоты собираются и охлаждаются, чтобы получить концентрированную кислоту в форме жидкости.
Некоторые неорганические кислоты могут быть получены путем окисления соответствующих неорганических соединений. Например, серная кислота может быть получена путем окисления серы. Для этого процесса может потребоваться использование специальных катализаторов и определенных температурных условий.
В зависимости от назначения неорганической кислоты, может потребоваться проведение дополнительных операций, таких как фильтрация и очистка. Эти операции позволяют удалить нечистоты и получить кислоту высокой чистоты.
Общий процесс получения неорганических кислот является сложным и требует строгого контроля параметров, таких как температура, давление и концентрация веществ. Также важным этапом является безопасность, поскольку некоторые неорганические кислоты могут быть коррозивными или ядовитыми. Поэтому все операции должны проводиться с соблюдением соответствующих мер предосторожности.








