Нециклические углеводороды представляют собой класс органических соединений, которые не образуют кольцевые структуры. В отличие от циклических углеводородов, такие соединения имеют прямую цепь атомов углерода. Они включают в себя моноциклические (содержащие одну цепь) и полициклические (содержащие несколько цепей) углеводороды.
Нециклические углеводороды обладают рядом уникальных свойств. Во-первых, они обычно являются наиболее простыми и наиболее распространенными типами углеводородов. Во-вторых, они могут быть разделены на несмешивающиеся фракции на основе их растворимости. Это свойство может быть использовано для их очистки и концентрирования. В-третьих, нециклические углеводороды обычно служат важными структурными блоками для синтеза других более сложных органических соединений.
Применение нециклических углеводородов в различных отраслях науки и промышленности очень широко. Они используются как растворители, реагенты для органического синтеза, компоненты косметических и фармацевтических препаратов, а также в процессах добычи нефти и газа. Их структурные особенности и разнообразие возможных функциональных групп делают их универсальными строительными блоками для создания сложных молекул и материалов.
Нециклические углеводороды: определение
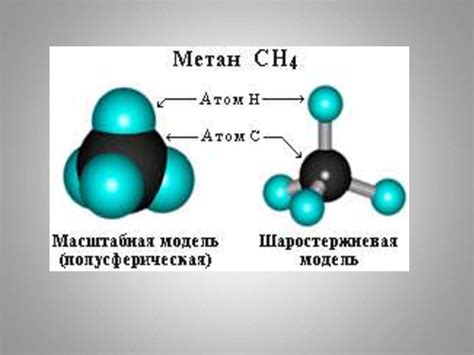
Нециклические углеводороды представляют собой класс органических соединений, состоящих из атомов углерода и водорода, где атомы углерода соединены в одну прямую цепь. Также известны как алифатические (линейные) углеводороды.
Главным отличием нециклических углеводородов от их циклических аналогов является то, что у них нет замкнутых колец атомов углерода. Вместо этого, атомы углерода образуют открытую цепь, которая может быть прямой или разветвленной. Такая структура позволяет нециклическим углеводородам образовывать различные конфигурации и изомеры.
Нециклические углеводороды могут быть классифицированы по количеству связей между атомами углерода:
- Насыщенные углеводороды содержат только одинарные связи между атомами углерода. Примером таких соединений является пропан - углеводород с тремя атомами углерода и восемью атомами водорода.
- Ненасыщенные углеводороды содержат двойные или тройные связи между атомами углерода. Примером таких соединений является этилен - углеводород с двумя атомами углерода и четырьмя атомами водорода, содержащий две двойные связи.
Нециклические углеводороды находят широкое применение в различных областях, включая пищевую, фармацевтическую, косметическую и полимерную промышленность. Их свойства и реакционная способность определяют их функциональное использование и важность в органической химии.
Что такое нециклические углеводороды?
Нециклические углеводороды широко представлены в природе и являются основой многих органических соединений. В основном они получаются из нефти или природного газа и используются в различных отраслях промышленности.
- Насыщенные нециклические углеводороды, такие как метан, этан и пропан, являются газообразными при нормальных условиях.
- Ненасыщенные нециклические углеводороды, такие как этилен, пропилен и бутадиен, обладают двойными или тройными связями между атомами углерода и могут быть газообразными, жидкими или твердыми веществами.
Нециклические углеводороды являются важными промышленными сырьем для производства пластиков, синтетических волокон, лекарств, красителей, растворителей и других продуктов.
Структура нециклических углеводородов
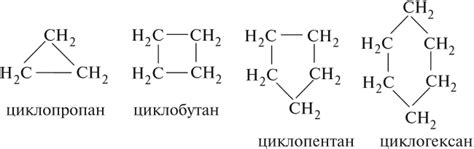
Структура нециклических углеводородов определяется количеством углеродных атомов в цепи и типом связей между ними.
Простейшим типом нециклического углеводорода является метан (CH4). Он состоит из одного углеродного атома, связанного с четырьмя водородными атомами:
CH4
Другим примером нециклического углеводорода является энтан (C2H6). Он состоит из двух углеродных атомов, связанных с шестью водородными атомами:
CH3CH3
Нециклические углеводороды могут быть длинными цепями, включающими множество углеродных атомов. Например, пропан (C3H8) имеет три углеродных атома в цепи:
CH3CH2CH3
Структура нециклических углеводородов определяет их свойства и применение. Они могут быть использованы в производстве пластиков, резин, лаков, красителей, моющих средств и других продуктов.
Свойства нециклических углеводородов
Нециклические углеводороды, также известные как алифатические углеводороды, обладают рядом характеристик, которые делают их уникальными и востребованными в различных сферах.
Вот некоторые из основных свойств нециклических углеводородов:
- Гибкость: Нециклические углеводороды обладают гибкой структурой, что делает их способными к образованию разнообразных химических соединений.
- Реакционная способность: Нециклические углеводороды обладают большой реакционной способностью, что делает их полезными в органическом синтезе.
- Теплостойкость: Большинство нециклических углеводородов обладает высокой теплостойкостью, что делает их полезными в высокотемпературных процессах, таких как синтез полимеров.
- Воспламеняемость: Нециклические углеводороды имеют разную степень воспламеняемости в зависимости от их структуры и наличия функциональных групп. Это свойство может использоваться в различных применениях, включая производство топлива.
- Растворимость: Многие нециклические углеводороды растворимы в органических растворителях и нерастворимы в воде. Это делает их полезными в химической и фармацевтической промышленности.
- Токсичность: Некоторые нециклические углеводороды могут быть токсичными для организмов и окружающей среды. Поэтому при работе с ними необходимо соблюдать соответствующие меры предосторожности.
В целом, нециклические углеводороды обладают разнообразными свойствами и могут быть использованы во многих отраслях промышленности и научных исследований.
Физические свойства нециклических углеводородов
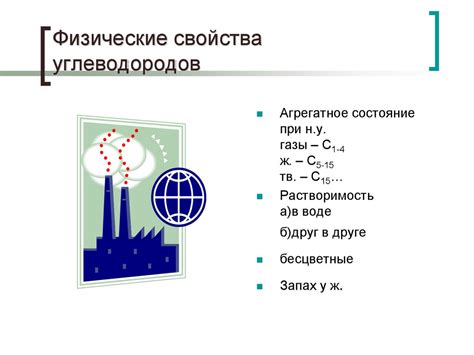
Нециклические углеводороды обладают рядом физических свойств, которые определяют их поведение и применение в различных областях.
Температура плавления и кипения: Нециклические углеводороды имеют разные температуры плавления и кипения, которые зависят от их молекулярной структуры и межмолекулярных взаимодействий. Например, алканы обладают более высокими температурами плавления и кипения, чем алкены и алкины с аналогичным числом углеродных атомов.
Теплоемкость: Нециклические углеводороды имеют разную теплоемкость, которая характеризует их способность поглощать тепло. Теплоемкость может быть использована для расчета количества тепла, необходимого для изменения температуры вещества.
Плотность: Плотность нециклических углеводородов также различается и зависит от их молекулярной структуры и массы. Плотность может влиять на свойства растворов, такие как вязкость и плотность пара.
Растворимость: Растворимость нециклических углеводородов в различных растворителях может варьировать в зависимости от их полярности и межмолекулярных взаимодействий. Например, неполярные углеводороды обычно хорошо растворяются в других неполярных растворителях, таких как бензол, но плохо растворяются в полярных растворителях, например, воде.
Электрическая проводимость: Нециклические углеводороды обычно являются непроводящими электричество в чистом виде из-за отсутствия заряда. Однако, они могут обладать проводящими свойствами при наличии примесей или при изменении их структуры для получения кондуктивных полимеров.
Летучесть: Нециклические углеводороды обычно обладают высокой летучестью и могут быстро испаряться при комнатной температуре и давлении. Это свойство может быть использовано в различных процессах, таких как экстракция и дистилляция.
Физические свойства нециклических углеводородов играют важную роль в определении их производственных и промышленных применений. Знание этих свойств помогает в выборе и использовании углеводородов в различных областях, включая предпринимательство, науку и инженерию.
Химические свойства нециклических углеводородов
Нециклические углеводороды, также известные как алифатические углеводороды, обладают разнообразными химическими свойствами.
Первое и наиболее важное химическое свойство нециклических углеводородов - их способность к реакциям с окислителями. Углеводороды могут вступать в реакцию с кислородом, образуя соответствующие оксиды. При этом могут образовываться как полные окислы, так и не полные окислы, в зависимости от условий реакции.
Еще одно химическое свойство нециклических углеводородов - их способность к реакции с кислотами. Углеводороды могут взаимодействовать с кислотами, образуя соли или другие продукты реакции. Реакция может проходить как сильной кислотой, так и слабой кислотой, в зависимости от силы кислоты и условий реакции.
Также нециклические углеводороды могут вступать в реакцию с щелочами. При этом образуются соли углеводорода и соответствующие продукты реакции. Реакция может проходить с сильной щелочью, такой как натрия гидроксид, или слабой щелочью, такой как аммиак водный раствор.
Нециклические углеводороды также могут проходить реакцию с различными другими веществами, такими как алкоголи, карбонаты, галогены и т.д. Их реакционная способность зависит от структуры молекулы углеводорода и условий реакции.
| Химическое свойство | Описание |
|---|---|
| Окисление | Углеводороды могут вступать в реакцию с кислородом, образуя соответствующие оксиды. |
| Взаимодействие с кислотами | Углеводороды могут взаимодействовать с кислотами, образуя соли или другие продукты реакции. |
| Взаимодействие с щелочами | Углеводороды могут вступать в реакцию с щелочами, образуя соли углеводорода и соответствующие продукты реакции. |
| Взаимодействие с другими веществами | Углеводороды могут реагировать с различными другими веществами, такими как алкоголи, карбонаты, галогены и т. д. |








