Массовая концентрация – это физическая характеристика растворов, которая показывает количество растворенного вещества в единице объема или массы растворителя. Она является одним из ключевых понятий в химии и широко используется в аналитической химии, биохимии и других областях науки.
Формула для расчета массовой концентрации обычно записывается следующим образом: $$C = \frac{m}{V}$$ где $$C$$ - массовая концентрация, $$m$$ - масса растворенного вещества, а $$V$$ - объем растворителя.
Например, чтобы рассчитать массовую концентрацию соли в растворе, нужно знать массу соли и объем растворителя. Если масса соли равна 10 г, а объем растворителя составляет 500 мл, то массовая концентрация соли будет: $$C = \frac{10 \, г}{500 \, мл} = 0.02 \, г/мл$$
Массовая концентрация обычно выражается в граммах на миллилитр ($$г/мл$$) или в процентах ($$г/100мл$$). Важно отметить, что она может быть указана как вещества в растворе, так и растворителя. Например, массовая концентрация глюкозы в плазме крови может быть выражена как "массовая концентрация глюкозы в плазме" или "массовая концентрация плазмы крови в глюкозе".
Что такое массовая концентрация?

Массовая концентрация обычно выражается в г/л (граммах на литр) или мг/мл (миллиграммах на миллилитр). Например, если в 1 литре раствора содержится 10 граммов соли, то массовая концентрация этого раствора будет равна 10 г/л.
Массовая концентрация играет важную роль в различных областях науки и промышленности. Например, она широко используется в химии для определения степени разбавления растворов, контроля качества продукции или подготовки реагентов.
Формула для расчета массовой концентрации проста:
Массовая концентрация (г/л) = масса растворенного вещества (г) / объем растворителя (л)
Например, если нам известно, что в 500 мл раствора содержится 50 г соли, мы можем легко рассчитать массовую концентрацию:
Массовая концентрация = 50 г / 0,5 л = 100 г/л
Определение, значение и применение
Массовая концентрация (также известная как концентрация по массе или плотность) представляет собой количественную меру содержания одного вещества в другом веществе. Она выражается в массе вещества, находящегося в единице объема или массы другого вещества.
Значение массовой концентрации важно в различных областях науки и техники. Например, в химии она используется для определения степени разведения растворов, анализа состава и концентрации компонентов веществ. В биологии и медицине массовая концентрация применяется, например, для определения концентрации лекарственных препаратов в крови.
Для расчета массовой концентрации необходимо использовать определенную формулу. Если известна масса вещества и объем (или масса) растворителя, то массовая концентрация может быть вычислена по следующей формуле:
- Массовая концентрация = (масса вещества / объем растворителя) * 100%
Например, если в 500 мл воды растворено 10 г соли, то массовая концентрация соли в этом растворе будет равна (10 г / 500 мл) * 100% = 2%.
Знание массовой концентрации позволяет более точно оценивать свойства веществ и контролировать процессы, в которых они участвуют.
Формула массовой концентрации
массовая концентрация = (масса растворенного вещества) / (объем растворителя)
Где:
массовая концентрация - величина, выражающаяся в г/мл или г/л;
масса растворенного вещества - масса соли, растворенной в растворителе, выражается в граммах (г);
объем растворителя - объем растворителя, выражается в миллилитрах (мл) или литрах (л).
Например, если в 100 мл растворителя растворено 10 г соли, то массовая концентрация этого раствора будет равна 0,1 г/мл или 100 г/л.
Как вычислить массовую концентрацию?
Массовая концентрация указывает, сколько граммов растворенного вещества содержится в единице объема растворителя. Для того чтобы вычислить массовую концентрацию, необходимо знать массу растворенного вещества и объем растворителя.
Формула для вычисления массовой концентрации (с) выглядит следующим образом:
с = m / V
где:
с - массовая концентрация (г/л);
m - масса растворенного вещества (г);
V - объем растворителя (л).
Для примера, представим, что у нас есть раствор с массой NaCl равной 10 г и объемом воды равным 1 л. Чтобы вычислить массовую концентрацию NaCl в данном растворе, мы будем применять формулу:
с = 10 г / 1 л = 10 г/л
Таким образом, массовая концентрация NaCl в данном растворе составляет 10 г/л.
Примеры расчета массовой концентрации
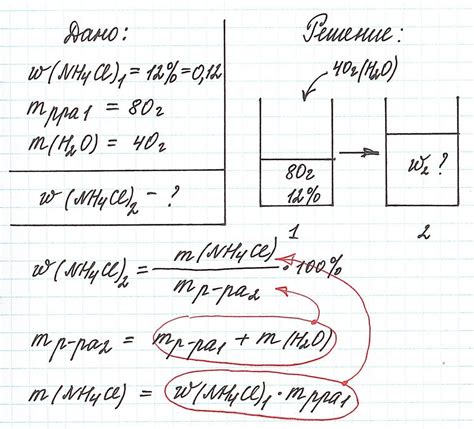
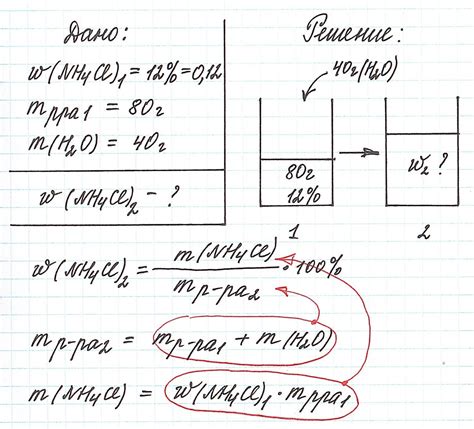
Ниже приведены несколько примеров для наглядного понимания расчета массовой концентрации.
Пример 1:
Рассчитайте массовую концентрацию воды в растворе, если вес раствора составляет 500 г, а масса воды в этом растворе составляет 300 г.
Используем формулу:
Массовая концентрация (массовая доля) = (Масса компонента / Общая масса раствора) * 100%
Массовая концентрация воды = (300 г / 500 г) * 100% = 60%
Пример 2:
Рассчитайте массовую концентрацию глюкозы в растворе, если масса раствора составляет 600 г, а масса глюкозы в этом растворе составляет 40 г.
Используем формулу:
Массовая концентрация (массовая доля) = (Масса компонента / Общая масса раствора) * 100%
Массовая концентрация глюкозы = (40 г / 600 г) * 100% = 6.67%
Пример 3:
Рассчитайте массовую концентрацию соли в растворе, если вес раствора составляет 800 г, а масса соли в этом растворе составляет 120 г.
Используем формулу:
Массовая концентрация (массовая доля) = (Масса компонента / Общая масса раствора) * 100%
Массовая концентрация соли = (120 г / 800 г) * 100% = 15%
Таким образом, массовая концентрация позволяет выразить отношение массы компонента к общей массе раствора в процентах.
Практические примеры и задачи
Рассмотрим несколько практических примеров и задач, связанных с массовой концентрацией:
- Пример 1: В 100 мл раствора содержится 5 г соли. Найдите массовую концентрацию данного раствора.
- Пример 2: Какая масса сульфата натрия нужна для приготовления 500 мл раствора с массовой концентрацией 0,1 г/мл?
- Пример 3: Найдите объем раствора, содержащего 15 г меди, если массовая концентрация раствора равна 0,2 г/мл.
Решение данных примеров и задач позволит лучше разобраться в применении массовой концентрации в реальных ситуациях.








