Внешний электронный слой является очень важным понятием в химии. Он состоит из электронов, которые находятся на самом внешнем уровне атома. Именно эти электроны определяют химическую активность элементов.
Внешний электронный слой играет роль в химических реакциях и связывании атомов между собой. Элементы с неполным внешним слоем стремятся заполнить его электронами путем образования химических связей с другими атомами. Таким образом, эти элементы обладают высокой химической активностью.
Например, атом хлора имеет 7 электронов во внешнем слое и стремится получить еще один электрон, чтобы заполнить свой внешний слой. Поэтому он будет активно реагировать с другими атомами, чтобы заполучить недостающий электрон и стать более стабильным.
С другой стороны, элементы с полностью заполненным внешним слоем обладают меньшей химической активностью. Например, атом гелия имеет 2 электрона во внешнем слое и полностью заполненный внутренний слой. Это делает его очень стабильным и менее реактивным.
Таким образом, значение внешнего электронного слоя состоит в его способности определять химическую активность элементов и их способность взаимодействовать с другими атомами для образования химических соединений.
Внешний электронный слой и химическая активность элементов
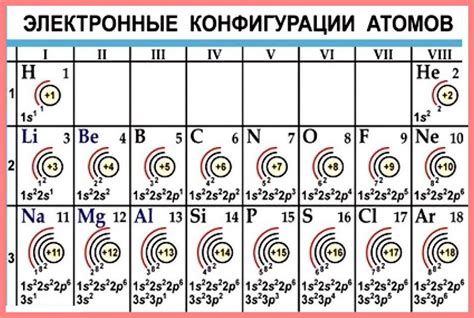
Валентные электроны играют важную роль в химических реакциях, так как они участвуют в образовании химических связей. Количество электронов на внешнем слое определяет, сколько электронов элемент может отдать или принять при взаимодействии с другими атомами, что определяет его химическую активность.
Элементы с полностью заполненным внешним слоем электронов имеют малую активность и обладают низкой реакционной способностью. К таким элементам относятся инертные газы, такие как гелий и неон.
Элементы, у которых внешний слой имеет не все электроны, но близко к заполнению, обладают высокой химической активностью. Отдавая или принимая несколько электронов, они стремятся заполнить или освободить внешний энергетический уровень.
Внешняя электронная конфигурация элементов позволяет классифицировать их по группам: главные группы и переходные металлы. Главные группы соответствуют собственно элементам, у которых внешний слой содержит s- и p-электроны, а переходные металлы - элементам, у которых внешний электронный слой заполнен частично d-электронами.
Внешний электронный слой и химическая активность элементов неразрывно связаны и определяют множество химических свойств атомов и их соединений. Изучение этих связей позволяет лучше понять причины реакционной способности различных химических элементов.
Роль внешнего электронного слоя в химической активности
Внешние электроны могут быть перешедшими на другой атом при химической реакции, образуя химическую связь. Количество внешних электронов определяет валентность атома и его способность образовывать химические связи.
Чем больше внешних электронов у атома, тем выше его химическая активность. Элементы с неполным электронным слоем, так называемые валентные элементы, обладают высокой химической активностью и легко образуют химические связи с другими элементами. Валентные электроны атома стремятся либо заполнить свой энергетический уровень, либо передать свои электроны атому с неполным слоем, чтобы в обоих случаях достичь более стабильного состояния.
Внешний электронный слой и валентность атома являются основными химическими характеристиками элементов и определяют их способность участвовать в реакциях с другими элементами. Благодаря различной валентности атомов, возможно образование разнообразных соединений и сложных молекул.
Внешний электронный слой является ключевым фактором в химической активности элементов и играет важную роль в образовании химических связей.
Значение количества электронов во внешнем электронном слое

Количество электронов во внешнем электронном слое атома играет важную роль в химической активности элементов. Внешний электронный слой содержит электроны, отвечающие за химические связи и реакции с другими атомами.
Если внешний электронный слой атома содержит малое количество электронов (1, 2, или 3), то элемент имеет склонность отдавать эти электроны и образовывать ионы положительного заряда. Такие элементы называются металлами и относятся к группе I, II и III периодической системы.
Напротив, если внешний электронный слой содержит больше электронов, элемент имеет склонность принимать электроны и образовывать отрицательно заряженные ионы. Такие элементы называются неметаллами и относятся к группе V, VI, и VII периодической системы, а также к группе 0 или VIII, известной как инертные газы.
Это свойство элементов связано с достижением электронной конфигурации, а именно с заполнением или освобождением внешнего электронного слоя. Одним из основных правил химической связи является стремление каждого атома к заполнению или освобождению своего внешнего слоя электронов, чтобы достичь более стабильной конфигурации, подобной электронной конфигурации инертных газов.
Таким образом, количество электронов во внешнем электронном слое атома определяет его реакционную способность, химическую активность и возможность образования связей с другими атомами, что в итоге определяет его место в периодической таблице.
Влияние внешнего электронного слоя на химические свойства элементов
Внешний электронный слой атома играет важную роль в определении его химической активности и свойств. Внешние электроны находятся на наиболее удаленных от ядра уровнях энергии и именно они взаимодействуют с другими атомами при химических реакциях.
Количество электронов во внешнем слое атома, также известное как валентность, определяет его способность к образованию химических связей с другими атомами. Атомы с полностью заполненным внешним электронным слоем, например инертные газы, обладают низкой химической активностью и малой склонностью к реакциям, так как им нет необходимости принимать или отдавать электроны.
В отличие от инертных газов, элементы с неполностью заполненным внешним электронным слоем, такие как металлы и неметаллы, обладают высокой химической активностью. Они стремятся достичь стабильности, заполнив внешний слой или избавившись от избытка электронов через образование химических связей с другими атомами.
Другой важной характеристикой внешнего электронного слоя является его форма. Атомы с разными формами внешних слоев могут иметь различную химическую активность и склонность к образованию определенных типов химических связей. Например, атомы с внешним слоем в форме s-орбитали обычно образуют ионические связи, а атомы с внешним слоем в форме p-орбитали чаще всего образуют ковалентные связи.
Внешний электронный слой также влияет на химические свойства элементов через эффекты экранирования и положительного заряда ядра. Внешние электроны экранируют внутренние слои от притяжения ядра, что делает валентные электроны более доступными для других атомов. Кроме того, внешние электроны также создают отрицательный заряд внешнего слоя, который компенсирует положительный заряд ядра. Это также способствует образованию химических связей и реактивности атома.
Таким образом, внешний электронный слой имеет огромное значение для химической активности элементов. Он определяет валентность атома, его способность к образованию химических связей и тип сформированных связей. Кроме того, внешний слой влияет через экранирование и положительный заряд ядра на химическую реактивность и свойства элементов.








