Молекулярное строение веществ - это ключевой аспект в изучении химии и физики. Вся материя в мире состоит из атомов, которые соединяются между собой, образуя молекулы. Молекулы, в свою очередь, имеют свою уникальную структуру и компоновку, которая определяет свойства и поведение вещества.
Концепция молекулярного строения разрабатывается на основе принципов квантовой механики и химической теории. Молекулярные связи, состоящие из электронов, помогают объединить атомы в молекулы и удерживают их в определенной форме. Форма и конфигурация молекулы сильно влияют на ее химические и физические свойства, такие как температура плавления, вязкость, проводимость и т.д.
Молекулярное строение также играет важную роль в биологических системах. Белки, ДНК и другие молекулы, составляющие живые организмы, имеют сложную трехмерную структуру, которая определяет их функции и возможности взаимодействия с окружающей средой. Молекулярный подход открывает новые возможности в медицине, генетике и фармацевтике, позволяя разрабатывать новые лекарства и методы лечения различных заболеваний.
Изучение молекулярного строения позволяет разобраться в том, как взаимодействуют различные вещества и какие изменения могут произойти при химических реакциях. Эта область науки играет фундаментальную роль в различных отраслях исследований и применений, от разработки новых материалов до создания новых технологий и развития экологически чистых процессов.
Определение и основные принципы

Молекулярное строение вещества относится к его составу и описывает, какие атомы и как они связаны друг с другом в молекулах. От молекулярной структуры зависят химические свойства вещества.
Основные принципы молекулярного строения можно выделить следующие:
- Атомная структура: каждая молекула состоит из атомов, которые образуют связи между собой.
- Связи между атомами: атомы соединяются между собой с помощью химических связей, которые могут быть ковалентными, ионными или металлическими.
- Геометрия молекулы: атомы в молекуле могут располагаться в определенном порядке и формировать различные геометрические формы, такие как линейные, плоские или трехмерные.
- Структурные формулы: для наглядного представления молекулярной структуры используются структурные формулы, где атомы изображаются символами, а связи между ними – линиями или точками.
- Молекулярные спектры: исследование молекулярных спектров помогает определить энергетическое состояние молекул и их строение.
Изучение молекулярного строения позволяет лучше понять химические реакции и свойства вещества, а также применять эту информацию в различных областях, таких как фармакология, материаловедение и биология.
Важность молекулярного строения для химических реакций
Молекулярное строение веществ играет важную роль в химических реакциях. Оно определяет свойства и поведение вещества во время химических превращений.
Молекулы состоят из атомов, которые связаны между собой определенными химическими связями. У каждого вида вещества могут быть различные типы связей и различные атомы, что влияет на характеристики вещества.
Молекулярное строение вещества определяет его полюсность, степень реакционной активности и способность образовывать новые соединения. Например, неметаллические элементы имеют молекулы, которые часто образуют ковалентные связи. В молекулярном строении вещества тоже может быть положительный и отрицательный заряды, что имеет значение для возможности образования ионных связей.
Молекулярное строение вещества также влияет на его растворимость и реакционную способность. Некоторые молекулы имеют полюсность и могут образовывать водородные связи с другими молекулами. Это позволяет им образовывать растворы, быть растворимыми в воде и участвовать в реакциях, таких как образование солей или обмен ионами.
Понимание молекулярного строения вещества позволяет предсказывать его поведение в различных химических реакциях и разрабатывать новые материалы и соединения с нужными свойствами. Изучение молекулярной структуры становится все более важным для дальнейшего развития химической науки и применения химических веществ в различных областях жизни.
Взаимосвязь молекулярного строения и свойств веществ
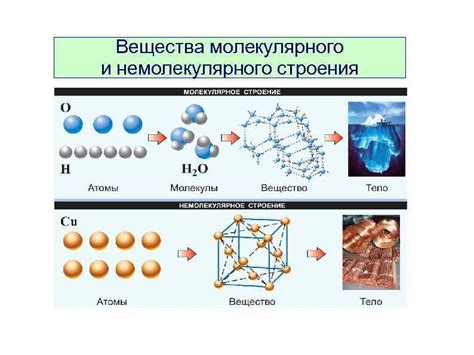
Одно из основных свойств веществ, определяемое их молекулярным строением, это физическое состояние. В зависимости от типа межмолекулярных взаимодействий и их силы, вещества могут находиться в твердом, жидком или газообразном состояниях. Например, вещества с сильными межмолекулярными силами, такими как ионные или ковалентные вещества, обычно находятся в твердом состоянии. В то же время, вещества с слабыми взаимодействиями, например, ван-дер-ваальсовыми силами, могут находиться в жидком или газообразном состоянии.
Еще одним важным свойством, зависящим от молекулярного строения вещества, является его температура плавления и кипения. Молекулы сильно связанных веществ обладают более высокими точками плавления и кипения, так как для разрушения их межмолекулярных связей требуется больше энергии. Напротив, молекулы слабо связанных веществ имеют более низкие температуры плавления и кипения, так как их межмолекулярные связи легче нарушаются.
Кроме того, молекулярное строение вещества может определять его химическую активность и реакционную способность. Наличие определенных функциональных групп в молекуле вещества может делать его легко реагирующим с другими веществами или способствовать протеканию определенных химических реакций. Например, наличие карбоксильной группы в молекуле кислоты позволяет ей образовывать соли с основаниями.
Одним из важных факторов, определяющих свойства вещества, является его поларность. Молекулы с неполярными связями обычно не обладают полярностью и не растворяются в полярных растворителях, таких как вода. В то же время, молекулы с полярными связями обладают полярностью и могут растворяться в полярных растворителях. Это свойство вещества определяется его молекулярным строением и типом связей между атомами.
Таким образом, молекулярное строение вещества играет важную роль в определении его свойств и поведения. Понимание взаимосвязи между молекулярным строением и свойствами веществ позволяет прогнозировать и объяснять их химическое и физическое поведение, а также разрабатывать новые материалы с определенными свойствами.
Методы исследования молекулярного строения
Одним из основных методов исследования молекулярного строения является рентгеноструктурный анализ. Суть этого метода заключается в том, что рентгеновские лучи проходят через кристалл и рассеиваются атомами, образуя определенную дифракционную картину, которую можно интерпретировать для определения положения атомов внутри кристаллической решетки.
Другим распространенным методом исследования молекулярного строения является ядерный магнитный резонанс (ЯМР). Этот метод основан на явлении ядерного магнитного резонанса, при котором ядра атомов взаимодействуют с внешним магнитным полем и излучают энергию в виде радиоволн. Путем анализа частоты и интенсивности излучения можно получить информацию о химической структуре и связях в молекуле.
Кроме того, широкое применение находят спектроскопические методы исследования молекулярного строения, такие как инфракрасная и УФ-видимая спектроскопия. Инфракрасная спектроскопия позволяет изучать колебательные и вращательные движения атомов внутри молекулы, а УФ-видимая спектроскопия - электронные переходы в молекуле.
Также стоит упомянуть масс-спектроскопию, которая позволяет определить массу и структуру молекулы на основе разделения ионов по массе и их детектирования.
Все эти методы, а также другие, позволяют ученым получать информацию о молекулярном строении вещества, что имеет важное значение для понимания его свойств и воздействия на окружающую среду.
Примеры веществ с различными молекулярными структурами
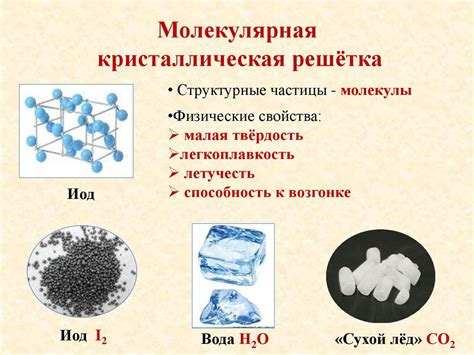
Вещества могут иметь различные молекулярные структуры, которые определяют их свойства и функции. Ниже приведены примеры веществ с различными молекулярными структурами:
- Вода (H2O): вода состоит из двух атомов водорода и одного атома кислорода, объединенных ковалентными связями. Молекула воды имеет угловую структуру с углом между атомами водорода около 104,5 градусов.
- Углекислый газ (CO2): молекула углекислого газа состоит из одного атома углерода и двух атомов кислорода, связанных двумя двойными связями. Молекула CO2 является линейной и не имеет полярности.
- Этан (C2H6): молекула этана состоит из двух атомов углерода и шести атомов водорода. Она имеет прямоугольную структуру с углом около 109,5 градусов между связями углерод-углерод и углерод-водород.
- Метан (CH4): молекула метана состоит из одного атома углерода и четырех атомов водорода. Молекула метана также имеет прямоугольную структуру с углом около 109,5 градусов между связями углерод-водород.
- Оксид азота (NO2): молекула оксида азота состоит из одного атома азота и двух атомов кислорода. Она имеет линейную структуру и является полярной молекулой.
Это лишь некоторые примеры веществ с различными молекулярными структурами. Молекулярное строение веществ является важным аспектом химии и оказывает влияние на их свойства и взаимодействия.








