Радиус атома – одно из важных понятий в химии, которое представляет собой расстояние от ядра атома до его наружной электронной оболочки. Этот параметр играет ключевую роль в определении физических и химических свойств атома, а также во многих процессах, связанных с реакциями между атомами.
Радиус атома определяется на основе процессов измерения и рассчитывается как половина расстояния между ядрами двух атомов в молекуле, когда эти атомы находятся в кристаллической решетке. Обычно радиус атома измеряется в ангстремах (1 А = 10^-10 метров).
Знание радиуса атома важно для понимания химической структуры вещества. Он влияет на такие химические свойства, как реакционная способность, способность образовывать химические связи и степень взаимодействия атомов в молекулах. Более того, радиус атома может служить основой для предсказания физических свойств, таких как температура плавления и кипения вещества.
«Знание радиуса атома является неотъемлемой частью химического исследования и играет важную роль в разработке новых материалов и лекарственных препаратов»
Что такое радиус атома?
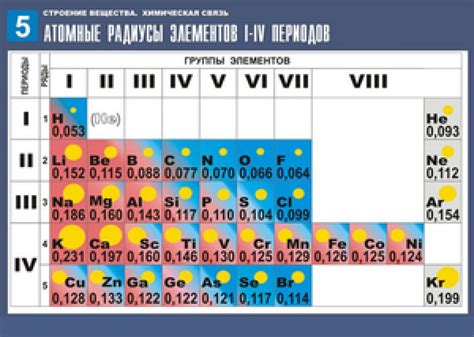
Радиус атома может варьироваться в зависимости от числа электронов и ядерных частиц в атоме. В общем случае, атомы становятся больше с увеличением числа электронов и ядерных частиц. Однако, радиус атома также может зависеть от других факторов, таких как химическое соседство и электронная конфигурация атома.
Радиус атома определяется экспериментально с использованием различных методов, таких как рентгеноструктурный анализ и спектроскопия. При измерении радиуса атома учитываются различные физические величины, такие как расстояние между ядром и электроном, эффективный радиус атома и другие. Поэтому, радиус атома может быть представлен различными значениями, которые зависят от выбранного метода измерения и используемой системы координат.
Знание радиуса атома позволяет понять, как могут взаимодействовать атомы друг с другом и формировать химические соединения. Например, маленькие атомы имеют большую электроотрицательность и могут образовывать ковалентные связи с другими атомами. Большие атомы, в свою очередь, имеют более слабую электроотрицательность и могут образовывать ионные связи. Размеры радиусов атомов также могут объяснить, почему некоторые вещества обладают определенными свойствами, такими как проводимость тока или пластичность.
В целом, радиус атома является важной величиной в химии, которая помогает понять структуру и свойства вещества. Он является основой для изучения многих химических явлений и может быть использован в различных приложениях, от разработки новых материалов до создания медикаментов.
Как определяется радиус атома?
Один из самых распространенных методов измерения радиуса атома - рентгеноструктурный анализ. В этом методе атомы вещества рассеивают рентгеновские лучи, и по результатам их дифракции можно рассчитать расстояния между атомами и, соответственно, радиусы атомов. Этот метод позволяет определить радиусы атомов с высокой точностью.
Еще одним способом определения радиуса атома является измерение его величины с помощью атомных силовых микроскопов. В таких микроскопах атомный зонд сканирует поверхность вещества, и измерение происходит на основе взаимодействия атомных сил, возникающих между зондом и поверхностью. Этот метод позволяет определить радиусы атомов с высоким разрешением.
Кроме того, радиус атома может быть рассчитан теоретически на основе данных о массе атома и его электронной конфигурации. Такие расчеты основаны на моделях атома, например, модели Шредингера. Теоретические значения радиусов атомов часто используются в химических расчетах.
Важно понимать, что радиус атома может меняться в зависимости от химического элемента и его окружения. Например, радиус атома может увеличиваться или уменьшаться при образовании химических связей. Поэтому радиус атома - это динамическая величина, которая может варьироваться в различных химических соединениях и структурах.
Какие факторы влияют на радиус атома?
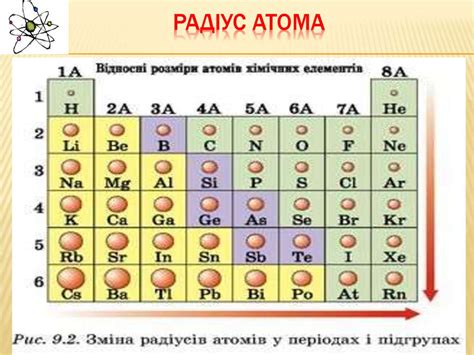
Радиус атома зависит от нескольких факторов:
- Атомный номер элемента: чем больше атомный номер, тем больше радиус атома.
- Количественное распределение электронов: с увеличением количества электронов радиус атома увеличивается.
- Заряд ядра: с увеличением заряда ядра (протонов) радиус атома уменьшается.
- Электронная конфигурация: способ распределения электронов в энергетических уровнях оказывает влияние на радиус атома.
- Образование ионов: ионизация атома может изменить его радиус.
- Эффект экранировки: некоторые электроны внутренних энергетических уровней могут экранировать электроны внешних энергетических уровней от притяжения ядра, что приводит к увеличению радиуса атома.
Все эти факторы взаимосвязаны и определяют размер атома в химических соединениях и элементах.
Значение радиуса атома в химии
Значение радиуса атома имеет огромное значение для понимания и прогнозирования реакций и свойств веществ. Он позволяет определить, как атомы расположены друг относительно друга в молекуле и какие взаимодействия между ними возможны.
Знание радиуса атома помогает установить размерные ограничения в химических реакциях. Например, если радиус атома слишком велик, то он может не поместиться в определенную решетку кристалла или в молекулу. Это может привести к невозможности проведения реакции или изменению структуры вещества.
Значение радиуса атома также влияет на химические свойства элемента. Например, размер атома может влиять на его способность образовывать связи с другими элементами. Если атом слишком большой, то связь может быть нестабильной или вообще не образовываться. С другой стороны, маленький радиус атома может привести к образованию очень сильных связей.
Таким образом, значение радиуса атома играет важную роль в химии. Оно определяет взаимодействие атомов друг с другом и веществ с окружающей средой. Использование данных о радиусе атома позволяет более точно понимать и описывать химические процессы.








