Растворы являются основными объектами изучения в химии и имеют широкое применение в различных областях науки и техники. Понять и измерить концентрацию растворов является важной задачей для химиков, биологов, медиков и многих других специалистов. Существует несколько основных методов, которые позволяют определить концентрацию растворов и измерить их количество вещества.
Одним из основных методов определения концентрации растворов является метод титрования. Этот метод основан на реакции между раствором, содержащим известное количество вещества, и раствором неизвестной концентрации. При добавлении титранта, который образует с реагентом вещество, отличающееся своими свойствами (например, изменением цвета), происходит изменение свойств раствора. Определение концентрации раствора производится путем измерения добавленного титранта.
Другим распространенным методом определения концентрации растворов является метод спектроскопии. Этот метод основан на использовании эффектов, связанных с взаимодействием электромагнитного излучения с веществом. При прохождении излучения через раствор или поглощении его раствором происходит изменение характеристик излучения, которые могут быть измерены специальными устройствами. По полученным данным можно оценить концентрацию раствора.
Итак, определение и измерение концентрации растворов является важной задачей в химии и других научных областях. Для этого существуют различные методы, такие как титрование и спектроскопия, которые позволяют достичь точных результатов. Правильное определение концентрации растворов позволяет проводить более точные и надежные исследования, а также использовать растворы в различных технических процессах.
Определение растворов и измерение их концентрации

Один из самых простых методов - измерение массы растворимого вещества. Для этого измеряют массу самого раствора, а затем высушивают его до полного удаления растворителя и снова измеряют массу. Разница между начальной и конечной массой будет соответствовать массе растворенного вещества.
Другой метод основан на изменении свойств раствора в зависимости от его концентрации. Например, можно измерить электрическую проводимость раствора, которая будет меняться в зависимости от концентрации растворенных ионов. Также можно использовать методы оптического анализа, например, изменение поглощения света при определенной длине волны.
Для измерения концентрации раствора также часто используют методы титрования. Данный метод основан на реакции между раствором неизвестной концентрации и известным реагентом. Путем добавления реагента, пока не достигнется эквивалентное соотношение, можно определить концентрацию исследуемого раствора.
Важно помнить, что для определения концентрации раствора необходимо учитывать факторы, такие как температура, давление и pH-значение раствора. Эти факторы могут оказывать влияние на реакцию между реагентами и исследуемым раствором, поэтому при выполнении опытов следует контролировать эти условия.
В целом, определение растворов и измерение их концентрации являются важной частью химического анализа. Правильная определение концентрации раствора позволяет проводить точные эксперименты и вычисления, а также применять полученные данные в разных областях науки и техники.
Методы анализа растворов в химии
Один из наиболее распространенных методов анализа растворов – гравиметрический метод, основанный на измерении массы выпавших соединений. Для этого раствор анализируется с помощью реакции с реагентом, образующим твердое вещество, которое затем фильтруется, осаждается и взвешивается. Измерив массу осадка, можно определить его концентрацию в исходном растворе.
Другой метод анализа – титриметрический. Он основывается на определении концентрации вещества в растворе путем реакции с реагентом-титрантом. В этом случае известный объем титранта добавляют в раствор и определяют точку эквивалентности, когда реакция полностью завершается. С помощью медицинского прибора, такого как бюретка, можно определить точное количество титранта, используемого для достижения точки эквивалентности, и тогда можно рассчитать концентрацию компонента в растворе.
Ионно-селективные электроды - это метод, основанный на измерении электрического потенциала разности между исследуемым раствором и стандартным раствором. Этот метод позволяет измерять концентрацию ионов в растворе, таких как водородные ионы, ионы кальция или натрия, с высокой точностью и быстротой.
Спектрофотометрия - это метод анализа, основанный на измерении поглощения или пропускания света через изучаемый раствор. Используя закон Бугера-Ламберта, можно определить концентрацию компонента в растворе, измерив его оптическую плотность с помощью спектрофотометра. Таким образом, можно измерить концентрацию различных соединений, таких как пигменты, органические кислоты и многое другое.
Это только некоторые из методов анализа растворов, используемых в химическом анализе. Каждый метод имеет свои преимущества и ограничения, и выбор метода зависит от требований конкретного исследования и доступных инструментов и ресурсов.
| Метод | Принцип | Преимущества | Ограничения |
|---|---|---|---|
| Гравиметрический | Измерение массы осадка | Высокая точность | Длительное время анализа |
| Титриметрический | Измерение объема реагента-титранта | Быстрота анализа | Точность зависит от умения оператора |
| Ионно-селективные электроды | Измерение электрического потенциала | Высокая точность и быстрота | Дорогие электроды |
| Спектрофотометрия | Измерение оптической плотности | Быстрота и широкий диапазон анализа | Требует калибровки и качественных стандартных образцов |
Спектрофотометрия в анализе растворов

Основной принцип работы спектрофотометра заключается в прохождении света через раствор и измерении интенсивности прошедшего света. Раствор поглощает определенную длину волны света в зависимости от своей концентрации. Измерение поглощения света позволяет определить концентрацию вещества в растворе.
Для проведения спектрофотометрического анализа необходимо подготовить образец раствора и поместить его в кювету спектрофотометра. Затем производится настройка спектрофотометра на определенную длину волны, которая соответствует поглощению выбранного вещества. После этого измеряется интенсивность света, прошедшего через раствор.
Интенсивность света в спектрофотометрии измеряется в оптических единицах - абсорбциях. Абсорбция рассчитывается по формуле A = log(I0/I), где A - абсорбция, I0 - интенсивность падающего света, I - интенсивность прошедшего света.
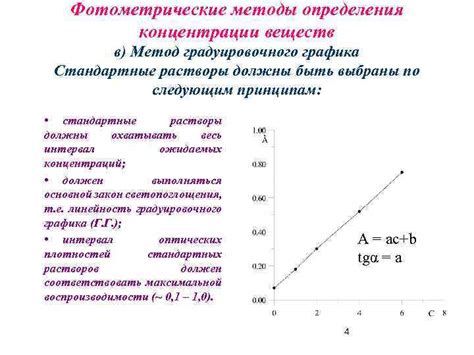
На основе полученных данных об абсорбции можно построить график зависимости абсорбции от концентрации вещества в растворе. Этот график называется калибровочной кривой. Калибровочная кривая позволяет определить концентрацию неизвестного образца, измерив его абсорбцию и находя соответствующее значение на графике.
Спектрофотометрия является одним из наиболее распространенных методов анализа растворов. Этот метод применяется в различных областях, например, в химическом анализе, биохимии, медицине и фармакологии, пищевой промышленности и др. Благодаря своей точности и высокой чувствительности спектрофотометрия позволяет получать качественные и количественные данные о составе и свойствах растворов.
Титриметрические методы измерения концентрации растворов
Существуют разные виды титриметрических методов, которые применяются в зависимости от химических свойств исследуемого раствора:
- Кислотно-основное титрование: используется для определения концентрации кислоты или щелочи в растворах. Кислотный или щелочной раствор взаимодействует с раствором стандартной кислоты или щелочи, и измерение объёма необходимого для нейтрализации позволяет рассчитать концентрацию исследуемого раствора.
- Окислительно-восстановительное титрование: используется для определения концентрации окислительного или восстановительного вещества в растворах. Исследуемое вещество взаимодействует с раствором стандартного окислительного или восстановительного вещества, и измерение объёма необходимого для полного окисления или восстановления позволяет рассчитать концентрацию исследуемого раствора.
- Прямое титрование: используется для определения концентрации веществ, которые могут прямо взаимодействовать с реагентом стандартного раствора. Измерение объёма стандартного раствора, необходимого для реакции с исследуемым веществом, позволяет рассчитать концентрацию исследуемого раствора.
- Комплексообразовательное титрование: используется для определения концентрации веществ, которые способны образовывать комплексы с реагентом стандартного раствора. Измерение объёма стандартного раствора, необходимого для образования комплекса с исследуемым веществом, позволяет рассчитать концентрацию исследуемого раствора.
Титриметрические методы измерения концентрации растворов широко применяются в аналитической химии и имеют высокую точность и воспроизводимость результатов. Они позволяют определить концентрацию растворов с высокой степенью точности и обеспечивают возможность контроля качества продукции в различных промышленных и научных областях.
Гравиметрические методы определения растворов

Гравиметрические методы определения растворов основаны на измерении массы вещества, образующегося в результате химической реакции. Эти методы широко используются в аналитической химии для определения концентрации различных веществ в растворах.
Главным принципом гравиметрических методов является тот факт, что масса образовавшегося вещества прямо пропорциональна концентрации анализируемого компонента в растворе. Поэтому путем измерения массы образовавшегося вещества можно определить его концентрацию в исходном растворе.
Одним из примеров гравиметрического метода является метод осаждения. При этом методе анализируемый компонент взаимодействует с определенным реагентом в растворе, образуя инертное осадок. Затем этот осадок отделяется, осушается и взвешивается. Масса осадка дает нам информацию о концентрации анализируемого компонента в исходном растворе.
Другим примером гравиметрического метода является метод титрования. При этом методе используется титрование раствора анализируемого компонента известным количеством реагента. После реакции происходит образование осадка, который после отделения и осушивания взвешивается. Масса осадка позволяет определить концентрацию анализируемого компонента в исходном растворе.
Гравиметрические методы определения растворов являются точными и надежными, так как измерения массы вещества достаточно точны и стабильны. Однако, эти методы требуют тщательной очистки и обработки образцов, а также продолжительного времени для проведения опытов. Кроме того, гравиметрические методы не всегда применимы для измерения низких концентраций анализируемых компонентов.
Электрохимические методы анализа растворов
Электрохимические методы анализа растворов представляют собой современные и широко используемые методы определения концентрации химических веществ в растворах. Они основаны на измерении электрических характеристик в процессе электрохимических реакций.
Одним из основных электрохимических методов анализа является вольтамперометрия, основанная на измерении электрического тока, проходящего через электрод. Вольтамперометрия позволяет определить концентрацию анализируемого вещества, основываясь на зависимости тока от потенциала на электроде. Этот метод применяется для определения таких характеристик растворов, как концентрация ионов, реакционная активность и другие электрохимические параметры.
Другим электрохимическим методом анализа является потенциостатический метод, который основан на поддержании постоянного потенциала на электроде. Путем изменения потенциала и измерения соответствующих токов можно определить концентрацию вещества в растворе. Этот метод широко применяется для анализа растворов с высокой точностью и чувствительностью.
Другие электрохимические методы анализа включают амперометрию, хроматическую вольтамперометрию, поларографию и ионоселективные методы. Каждый из этих методов имеет свои особенности и используется для анализа конкретных типов растворов и веществ.
Электрохимические методы анализа растворов обладают рядом преимуществ, включая высокую точность и чувствительность, быстроту и возможность работы с низкими концентрациями веществ. Кроме того, они могут быть автоматизированы и использованы для множества промышленных и лабораторных приложений.
В заключение, электрохимические методы анализа растворов представляют собой эффективные и надежные инструменты для определения концентрации химических веществ. Они позволяют проводить анализ с высокой точностью и чувствительностью, а также обладают широким спектром применения в различных областях науки и промышленности.
Аналитические методы определения концентрации растворов
Одним из самых распространенных методов является титрование. В данном методе объем раствора неизвестной концентрации добавляют постепенно к раствору с известной концентрацией (обычно с помощью бюретки) до достижения эквивалентной точки. Эквивалентная точка обычно определяется с помощью индикатора, который меняет цвет при достижении точки эквивалентности. Результаты титрования могут быть использованы для определения концентрации неизвестного раствора.
Другим методом анализа является спектрофотометрия. В данном методе измеряется поглощение или прохождение света через раствор при определенной длине волны. Концентрация раствора может быть определена на основе закона Бугера-Ламберта, который связывает концентрацию анализируемого вещества с поглощением света.
Еще одним методом является электрохимический анализ, который основан на использовании электродов и измерении электрической или электромагнитной характеристики раствора. Например, в методе потенциометрии измеряется разность потенциалов между электродами, что позволяет определить концентрацию раствора. Электрохимический анализ широко используется в определении концентрации ионов в растворах.
Кроме того, существуют и другие методы, такие как кулометрия, гравиметрический анализ, хроматография и др., которые также могут быть использованы для определения концентрации растворов.
Ионный хроматограф в анализе растворов
Основное преимущество ионного хроматографа состоит в его способности разделить различные ионы в растворе и определить их концентрацию. Это позволяет исследователям анализировать состав раствора и определять наличие и количество различных веществ в нем.
Процесс анализа раствора с помощью ионного хроматографа заключается в пропуске раствора через колонку с ионообменной смолой. Ионы, содержащиеся в растворе, взаимодействуют с колонкой, их разделяют по типу и заряду. Затем ионы проходят через детектор, который регистрирует их наличие и количество.
Одним из наиболее распространенных применений ионного хроматографа является анализ водных растворов на содержание различных ионов, таких как катионы (например, ионы натрия, калия, кальция) и анионы (например, нитраты, сульфаты, хлориды). Это предоставляет информацию о качестве питьевой воды, а также о содержании различных веществ в промышленных отходах и сточных водах.
Использование ионного хроматографа в анализе растворов позволяет проводить точные и надежные измерения концентрации ионов в растворах. Этот метод анализа является важным инструментом для многих областей, включая экологию, пищевую промышленность, фармацевтику и другие.
Масс-спектрометрия в анализе концентрации растворов

Процесс масс-спектрометрии включает несколько основных этапов. В начале происходит ионизация образца раствора с помощью высокоэнергетического лазерного излучения или других методов. Полученные ионы затем ускоряются в электрическом поле и разделяются по массе в магнитном поле, что позволяет получить масс-спектр, где каждый ион соответствует отдельному фрагменту молекулы вещества.
Для определения концентрации вещества в растворе по масс-спектру используется метод калибровки. Сначала проводится анализ растворов с известными концентрациями вещества, и для каждой концентрации строится калибровочная кривая, которая связывает интенсивность сигнала масс-спектра с концентрацией вещества. Затем, анализируя раствор с неизвестной концентрацией, можно использовать калибровочную кривую для определения его концентрации.
Масс-спектрометрия имеет множество преимуществ, таких как высокая чувствительность, точность и возможность анализа широкого диапазона веществ. Однако, она требует использования специализированного оборудования и опыта в интерпретации полученных данных. Поэтому, для проведения анализа концентрации растворов с помощью масс-спектрометрии рекомендуется обращаться к специалистам и лабораториям, обладающим необходимым оборудованием и опытом.








