В последнее время мы все чаще сталкиваемся с надписью "для клинических исследований" на различных продуктах и препаратах. Но что она на самом деле означает? Эта надпись указывает на то, что данное вещество или препарат прошел все необходимые лабораторные исследования и готов к тестированию на людях.
Клинические исследования - это специальные исследования, проводимые с целью выявления эффективности и безопасности новых препаратов, технологий или методов лечения. Они необходимы для получения достоверной информации о действии и потенциальных побочных эффектах нового продукта.
Прежде чем начать клинические исследования, необходимо провести тщательное лабораторное тестирование на моделях животных, чтобы убедиться в отсутствии токсичности и негативных эффектов. Если результаты лабораторных исследований будут положительными, препарат переходит на следующий этап - клинические исследования на добровольцах.
Важно понимать, что участие в клинических исследованиях является добровольным и подразумевает получение информированного согласия от каждого участника. Кроме того, такие исследования проводятся в строгом соответствии с международными этическими стандартами и регулируются специальными комитетами.
В процессе клинических исследований участники могут быть случайным образом разделены на группы, одна из которых получает новый препарат, а другая - плацебо или уже существующее лечение. Затем проводятся наблюдения за изменениями состояния здоровья, собираются данные и анализируются результаты.
Таким образом, надпись "для клинических исследований" указывает на то, что данный препарат или продукт еще находится в стадии проверки и требует дополнительных исследований на людях для того, чтобы подтвердить его эффективность и безопасность.
Что обозначает термин "для клинических исследований"?
Термин "для клинических исследований" указывает на то, что данный продукт или препарат еще не прошел полное клиническое испытание и не получил официального одобрения для использования в медицинской практике. Такие препараты, как правило, используются только в рамках клинических исследований, где они подвергаются тщательной оценке и изучению их эффективности и безопасности.
| Преимущества использования "для клинических исследований" | Недостатки использования "для клинических исследований" |
|---|---|
| - Позволяет провести контролируемое исследование на людях | - Не имеет официального одобрения для использования |
| - Позволяет изучить эффективность и безопасность продукта | - Может иметь побочные эффекты и неизвестные риски |
| - Может быть доступен пациентам, которым нет других лечебных альтернатив | - Может ограничиваться протоколами и исключать некоторые пациентские группы |
Надпись "для клинических исследований" на продукте напоминает о том, что его использование должно быть осуществлено только в рамках специальных исследований, с согласия пациента и под наблюдением медицинских специалистов.
Понятие исследовательского
Цель исследовательских исследований - расширить наши знания о конкретной проблеме или явлении. Они позволяют ученым исследовать, анализировать и интерпретировать данные и получать новые выводы и гипотезы.
Для клинических исследований эти исследования имеют особую важность, поскольку они направлены на изучение медицинских методов, процедур и лекарственных препаратов. Они позволяют ученым определить эффективность новых методов лечения, выявить побочные эффекты и риски, а также подтвердить эффективность и безопасность клинических интервенций.
Для проведения клинических исследований обычно требуется участие добровольцев, которые соглашаются принять участие в исследовании. Они могут быть подвержены новым методам лечения, медикаментозной терапии или протоколам наблюдения.
Исследовательские исследования имеют большое значение для развития медицины и науки в целом. Они позволяют получить новые данные и знания, которые могут быть использованы для улучшения практики медицины и здравоохранения, а также для развития новых методов диагностики и лечения различных заболеваний.
Значение в медицинской сфере

Надпись "для клинических исследований" на медицинском продукте указывает на то, что данный продукт предназначен для использования исключительно в рамках клинических исследований. Эта надпись указывает на то, что данный продукт еще не прошел полную процедуру регистрации и разрешения на использование в медицинской практике.
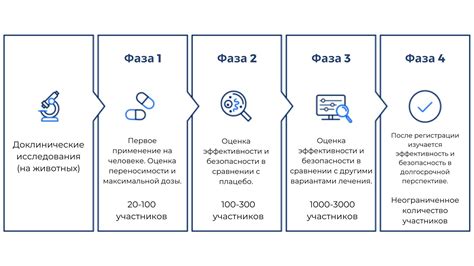
Клинические исследования являются одним из этапов разработки новых лекарственных препаратов, медицинских изделий и технологий. Они проводятся для определения эффективности и безопасности новых продуктов, а также для сравнительного анализа этих продуктов с уже существующими методами лечения. Клинические исследования включают в себя различные этапы, такие как фаза I (исследования на здоровых добровольцах), фаза II (предварительное изучение на ограниченной группе пациентов) и фаза III (широкомасштабное изучение на большой группе пациентов).
| Преимущества | Ограничения |
|---|---|
| Помогает определить эффективность и безопасность новых продуктов | Не гарантирует успешную регистрацию и разрешение на использование продукта в медицинской практике |
| Позволяет сравнить новые продукты с уже существующими методами лечения | Может быть связано с определенными рисками для пациентов |
| Предоставляет доступ к новым методам лечения и технологиям | Требует согласия и участия пациентов |
Таким образом, надпись "для клинических исследований" указывает на ограничение использования продукта только в рамках исследовательской деятельности и требует особой осторожности при его применении.
Требования к проведению
При проведении клинических исследований необходимо соблюдать следующие требования:
- Получение согласия от каждого участника исследования.
- Соблюдение этических принципов и конфиденциальности данных.
- Разработка протокола исследования, который включает описание целей, методологии и критериев.
- Проведение предварительных экспериментов и исследований на моделях перед переходом к клиническим тестам.
- Выбор репрезентативной группы участников исследования, учитывая особенности возраста, пола и состояния здоровья.
- Получение всех необходимых разрешений и лицензий от уполномоченных органов.
- Следование протоколу исследования на всех этапах, от сбора данных до анализа результатов.
- Учет различных факторов, которые могут повлиять на результаты исследования, таких как побочные эффекты или отклонения от протокола.
- Анализ и интерпретация полученных данных с использованием соответствующих статистических методов.
- Публикация результатов исследования для общественности и научного сообщества.
Этические аспекты

Проведение клинических исследований поднимает важные этические вопросы, связанные с защитой прав и благополучия участников исследования.
Одним из основных принципов в проведении клинических исследований является информированное согласие участника. Исследователи должны предоставить всю необходимую информацию о целях, ожидаемых результатах, возможных рисках и пользе от участия в исследовании, а также информацию о конфиденциальности данных и свободе от участия в исследовании.
Также важной частью этических принципов является справедливое распределение ресурсов и вознаграждение для участников. Участие в клинических исследованиях может быть связано с определенными рисками и неудобствами, поэтому здесь также возникают этические вопросы о честности и возможности получить положительные и психологические выгоды.
Кроме того, особое внимание уделяется конфиденциальности и защите данных участников исследования. Исследователи обязаны предпринять все необходимые меры для обеспечения конфиденциальности данных и защиты персональной информации участников.
Общественное доверие и этические нормы играют ключевую роль в успехе исследования. Раскрытие конфликта интересов, балансирование между научными и этическими потребностями и соблюдение кодексов этики помогают поддерживать доверие и этические стандарты в клинических исследованиях.








