Максимальная степень окисления - это важная характеристика химического элемента или соединения, которая определяет максимальное количество электронов, которое данное вещество может принять или отдать в химических реакциях. Она играет важную роль в определении его структуры, свойств и способности взаимодействовать с другими веществами.
Понятие максимальной степени окисления может быть очень полезным при изучении химии и химических реакций. Она позволяет предсказывать направление реакции и определить возможные продукты, которые могут образоваться. Знание максимальной степени окисления также помогает понять, как элементы образуют ионы и как электроны перемещаются во время реакции.
Высокая максимальная степень окисления может указывать на высокую активность элемента или соединения в химических реакциях. Например, хлор имеет максимальную степень окисления +7, что делает его очень реактивным и способным образовывать много соединений.
Знание максимальной степени окисления может быть полезным при изучении и применении химических реакций в различных областях, включая промышленность, медицину и экологию. Оно позволяет предсказывать и контролировать процессы, происходящие в различных веществах и системах. Поэтому понимание максимальной степени окисления является важным элементом химического образования и исследований.
Максимальная степень окисления: что это такое и почему важно
МСО играет важную роль в различных областях химии, таких как органическая, неорганическая и аналитическая химия. Она помогает определить химические свойства соединений и реакций, зная высшую степень окисления элемента в соединении.
Максимальная степень окисления влияет на реакционную способность и структуру соединений, и может указывать на возможные реакции и взаимодействия элементов. Знание МСО помогает предсказывать продукты химических реакций и понимать его химическую активность.
МСО также имеет большое значение в аналитической химии, так как может использоваться для идентификации и количественного определения элементов в соединениях. Зная МСО элемента в соединении, можно определить его концентрацию и химический состав.
В заключение, максимальная степень окисления является важным понятием в химии, которое помогает понять химические свойства соединений, идентифицировать элементы в соединениях и предсказывать химические реакции. Понимание МСО позволяет расширить наши знания и применять их в различных областях химической работы.
Определение максимальной степени окисления
МСО является важным понятием в химии, так как оно позволяет определить изменение зарядности атома при его окислении или восстановлении во время реакции. Чтобы определить МСО, необходимо знать электроотрицательности элементов и правила распределения электронов.
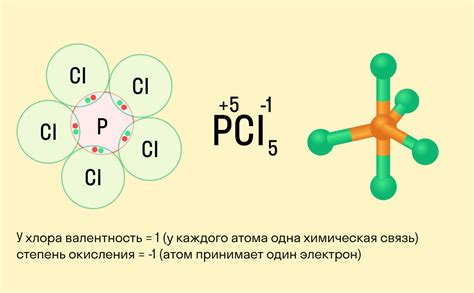
Максимальная степень окисления может быть положительной, если атом потерял электроны и стал положительно заряженным ионом. Например, в хлориде натрия (NaCl) натрий имеет МСО +1, так как он потерял один электрон и образовал ион Na+.
Максимальная степень окисления может быть отрицательной, если атом получил дополнительные электроны и стал отрицательно заряженным ионом. Например, в хлориде кальция (CaCl2) хлор имеет МСО -1, так как он получил один электрон и образовал ион Cl-.
Определение МСО помогает понять, какие элементы окисляются, а какие восстанавливаются в химической реакции. Это важно для понимания процессов, происходящих в органической и неорганической химии.
Значение максимальной степени окисления в химии

Значение максимальной степени окисления имеет большое значение для определения состава соединений, исследования реакций и прогнозирования их химических свойств. Он позволяет предсказать возможность различных окислительно-восстановительных процессов и определить роль вещества в реакции.
Таблица ниже приводит примеры значений максимальной степени окисления для некоторых элементов:
| Элемент | Максимальная степень окисления |
|---|---|
| Кислород (O) | -2 |
| Водород (H) | +1 |
| Хлор (Cl) | -1 |
| Железо (Fe) | +3 |
| Медь (Cu) | +2 |
Как видно из таблицы, для каждого элемента существует определенный диапазон значений максимальной степени окисления. Это связано с особенностями строения атомов и их электронной конфигурации.
Знание значений максимальной степени окисления позволяет химикам более точно прогнозировать химические реакции, а также исследовать электрохимические свойства соединений. Оно является основой для разработки новых материалов и применения в различных областях науки и техники.
Примеры максимальной степени окисления в различных соединениях
Вот несколько примеров различных соединений, где присутствует максимальная степень окисления:
- Вода (H2O): Максимальная степень окисления кислорода в этом соединении равна -2. Кислород само по себе имеет -2 МСО, поэтому вода называется оксидом водорода.
- Перекись водорода (H2O2): В перекиси водорода, МСО кислорода равна -1. Однако, МСО водорода здесь равна +1, что отличает перекись водорода от обычного водорода.
- Хлор (Cl2): МСО хлора в этом соединении равна 0, так как каждый атом хлора одинаково деляет электроны с другим атомом.
- Пятиокись дифосфора (P4O10): Здесь мы видим, что МСО фосфора равна +5, что означает, что фосфор активно окислен в данном соединении.
Эти примеры демонстрируют различные МСО в различных соединениях и помогают понять свойства и реактивность атомов в химических реакциях.
Влияние максимальной степени окисления на химические реакции
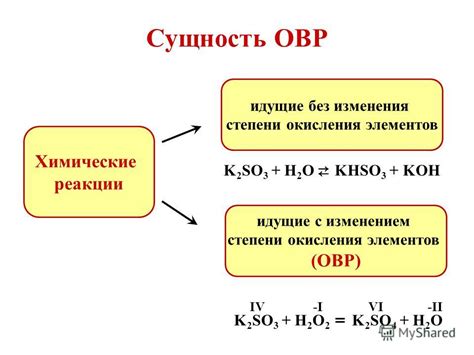
Максимальная степень окисления играет важную роль в химических реакциях, определяя характер и направление процесса. Химические реакции могут происходить как с участием окислителей, так и с участием восстановителей. Максимальная степень окисления элемента указывает на его способность принимать или отдавать электроны, что влияет на его реакционную активность.
Окислительно-восстановительные реакции являются одним из фундаментальных понятий в химии. Они происходят между веществами, в результате которых одно вещество окисляется, а другое восстанавливается. Максимальная степень окисления элемента определяет, какое количество электронов он может принять или отдать.
| Максимальная степень окисления: | Реакционная активность: | Примеры химических реакций: |
|---|---|---|
| +1 | Высокая | Взаимодействие редуцирующих агентов с окислителями |
| +2 | Умеренная | Образование солей, реакции кислот и оснований |
| +3 | Низкая | Реакции, в которых участвуют элементы из группы III |
| -2 | Высокая | Окисление водорода в гидридах |
| -1 | Умеренная | Реакции, в которых участвуют галогены |
Максимальная степень окисления элементов в различных соединениях позволяет предсказать их реакционную активность и способность участвовать в окислительно-восстановительных реакциях. Это важное понятие помогает установить тенденции и закономерности в химических реакциях, что является основой для разработки новых веществ и материалов.








