Когда мы говорим о реакциях, происходящих между химическими веществами, мы часто сталкиваемся с понятием "ионная форма реакции". Ионная форма реакции – это способ записи химической реакции, который позволяет описать присутствие ионов веществ в процессе взаимодействия. В отличие от обычной молекулярной формы реакции, ионная форма позволяет нам увидеть, какие ионы образуются и распадаются в процессе реакции.
Основной особенностью ионной формы реакции является использование зарядов ионов для написания уравнения. Заряды ионов указываются в виде индексов справа от знака элемента или в соответствующей нотации. Ионная форма реакции позволяет нам видеть, кто является катионом (положительно заряженным ионом) и кто анионом (отрицательно заряженным ионом) в процессе реакции. Это позволяет нам представить, какие ионы участвуют в образовании новых соединений и как происходит процесс переноса заряда.
Примером ионной формы реакции может быть реакция между хлороводородной кислотой (HCl) и гидроксидом натрия (NaOH), в ходе которой образуется хлорид натрия (NaCl) и вода (H2O). Ионная форма реакции для этого процесса будет выглядеть следующим образом: H+ + Cl- + Na+ + OH- -> Na+ + Cl- + H2O. В этом примере видно, что ионы водорода (H+), хлора (Cl-), натрия (Na+) и гидроксида (OH-) переходят из одной формы в другую.
Использование ионной формы реакции позволяет ученым более подробно изучать химические реакции и их механизмы, а также предсказывать, какие ионы будут образовываться и какие соединения возникнут при взаимодействии различных веществ. Ионная форма реакции играет важную роль в химической науке и помогает нам лучше понять мир химических соединений и их свойств.
Ионная форма реакции: определение и принципы действия
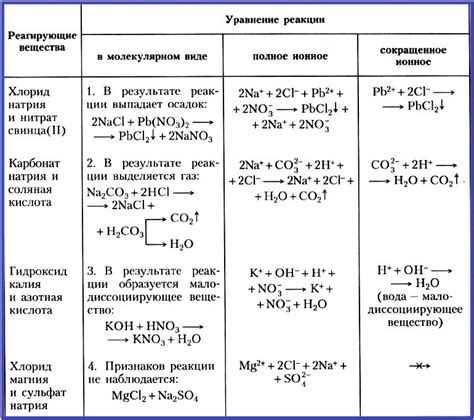
Для записи реакции в ионной форме используются коэффициенты, которые указывают на число ионов каждого вещества, участвующих в реакции. Ионная форма реакции позволяет более точно и подробно описать ионные переходы, электронные переносы и образование новых веществ.
Принципы действия ионной формы реакции:
- Реагенты записываются в ионной форме, указывая заряд ионообразующих элементов.
- Ионы могут быть положительными (катионами) или отрицательными (анионами), в зависимости от переноса электронов.
Пример ионной формы реакции:
| Ионная форма реакции | Обычная форма реакции |
|---|---|
| 2H+ + 2e- → H2 | H2 → 2H + 2e |
В приведенном примере ионной формы реакции видно, как водородион (H+) принимает два электрона (2e-), чтобы образовать молекулярный водород (H2).
Что такое ионная форма реакции?
Ионная форма реакции позволяет более точно описывать происходящие процессы и указывать, какие ионы участвуют в реакции и какие ионы образуются в результате. Такая запись позволяет более глубоко понять механизмы химических реакций и предсказывать их протекание.
Примеры ионной формы реакций могут быть следующими:
1) Реакция образования нитрата натрия:
NaOH + HNO3 → NaNO3 + H2O
Ионная форма: Na+ + OH- + H+ + NO3- → Na+ + NO3- + H2O
2) Реакция образования сернокислого меди:
2CuO + 2H+ → 2Cu2+ + H2O
Ионная форма: CuO + H+ → Cu2+ + H2O
Особенностью ионной формы реакции является то, что она показывает ионный состав веществ до и после реакции, что позволяет более точно определить количество электрических зарядов, участвующих в реакции.
Каковы особенности ионной формы реакции?

Основные особенности ионной формы реакции:
| 1. | Учет ионного состава. В ионной форме реакции указываются все ионы, образующиеся и исчезающие в результате реакции. Это позволяет уловить более полную картину происходящих изменений. |
| 2. | Отсутствие учета молекулярной структуры. При записи реакции в ионной форме не учитывается молекулярная структура вещества, а только ионные формулы и состояния ионов. Таким образом, иональная форма реакции упрощает запись и позволяет сосредоточиться на доле ионов в составе реагентов и продуктов. |
| 3. | Айонные уравнения. Ионная форма реакции позволяет составлять айонные уравнения, в которых указываются полные ионы, образующиеся в реакции. Это позволяет лучше понять, какие конкретно ионы участвуют в химической реакции. |
Примеры ионных форм реакций:
1. Реакция образования натрия(II) хлорида:
2Na(s) + Cl-(aq) → 2Na+(aq) + 2Cl-(aq)
2. Реакция образования серной кислоты:
H2O(l) + SO3(g) → H+(aq) + HSO4-(aq)
3. Реакция образования гидроксида натрия:
Na+(aq) + OH-(aq) → NaOH(aq)
Ионная форма реакции является важным инструментом в химии, позволяющим определять состав и структуру веществ, а также объяснять механизмы химических реакций.
Примеры ионных реакций
| Пример | Ионная форма реакции |
|---|---|
| Реакция образования соли | Na+ + Cl- → NaCl |
| Реакция нейтрализации | H+ + OH- → H2O |
| Реакция образования осадка | Ag+ + Cl- → AgCl(s) |
| Реакция окисления | Fe2+ → Fe3+ + e- |
| Реакция восстановления | Cr3+ + e- → Cr2+ |
Это лишь некоторые примеры ионных реакций. В реальности ионные реакции могут быть гораздо сложнее и включать большое количество ионов и реагентов.
Пример 1: образование осадка
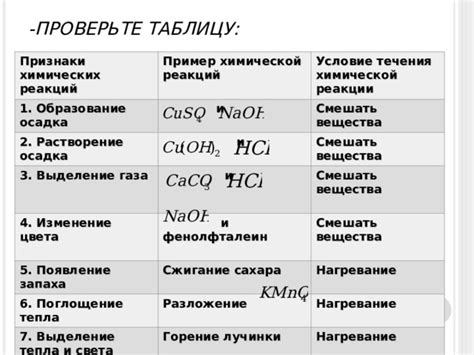
Например, при реакции между раствором нитрата серебра (AgNO3) и раствором хлорида натрия (NaCl) образуется осадок хлорида серебра (AgCl). Ионная форма этой реакции будет выглядеть следующим образом:
- Ag+ + NO3- + Na+ + Cl- → AgCl↓ + Na+ + NO3-
В данном случае ионы Ag+ и Cl- реагируют, образуя нерастворимый осадок AgCl. Этот пример демонстрирует, как ионная форма реакции позволяет описать происходящие химические превращения.
Пример 2: процессы обмена ионами
Один из примеров таких процессов - обмен протонами между кислотой и основанием. Например, реакция между соляной кислотой (HCl) и гидроксидом натрия (NaOH) представляет собой процесс обмена ионами:
- NaOH + HCl → NaCl + H2O
В этой реакции ионы Na+ и Cl- составляют гидрохлорид натрия (NaCl), а ионы H+ и OH- реагируют, образуя молекулу воды (H2O). Таким образом, происходит обмен ионами между кислотой и основанием.
Процессы обмена ионами также могут происходить в растворах, где ионы одного вещества замещают ионы другого вещества. Например, реакция между хлоридом бария (BaCl2) и сернокислым натрием (Na2SO4) приводит к образованию бария сульфата (BaSO4) и хлорида натрия (NaCl):
- BaCl2 + Na2SO4 → BaSO4 + 2NaCl
В этой реакции ионы Ba2+ и SO42- образуют барий сульфат (BaSO4), а ионы Na+ и Cl- образуют хлорид натрия (NaCl).
Такие процессы обмена ионами широко используются в химической промышленности, например, для получения различных соединений и очистки растворов от нежелательных ионов.








