Электроотрицательность - это химический параметр, который определяет способность атома притягивать электроны в химической связи. Более электроотрицательный элемент обладает большей силой притяжения электронов, чем менее электроотрицательный элемент.
Значение электроотрицательности заключается в его влиянии на химические связи. Когда два атома образуют химическую связь, электроотрицательность каждого элемента влияет на тип связи и ее силу. Более электроотрицательные элементы притягивают электроны к себе сильнее, что приводит к образованию полярной связи.
Например, водный молекула (H2O) образована соединением кислорода (O) и водорода (H). Кислород является более электроотрицательным элементом, поэтому он сильнее притягивает электроны, создавая положительный заряд около себя. Водород обладает меньшей электроотрицательностью и образует отрицательный заряд около себя.
Более электроотрицательные элементы также проявляют свою силу в молекулах, образуя полярные молекулы, в которых центральный атом обладает частичным зарядом. Это может влиять на физические свойства вещества, такие как температура плавления и кипения, растворимость и электропроводность.
Знание об электроотрицательности элементов является важным для понимания молекулярной структуры и связей между атомами. Оно помогает предсказать химические свойства веществ и использовать их в различных отраслях науки и промышленности, включая химию, биологию и материаловедение.
Понятие электроотрицательности

Более электроотрицательный элемент имеет большую способность притягивать электроны, чем менее электроотрицательный элемент. Самый электроотрицательный элемент - флуор, который имеет электроотрицательность 4,0 по шкале Полинга. Наоборот, самым менее электроотрицательным элементом является франций с электроотрицательностью 0,7.
Значение электроотрицательности определяется рядом факторов, включая количество электронов в атоме, их удаленность от ядра, а также размер атома. Чем меньше размер атома и чем больше его зарядовое число, тем более электроотрицательным он считается.
Электроотрицательность определяет химические свойства элементов и влияет на образование и характер химических соединений. Более электроотрицательные элементы имеют большую склонность к принятию электронов и образованию ионов, тогда как менее электроотрицательные элементы склонны отдавать электроны, образуя положительно заряженные ионы.
Зная значение электроотрицательности элементов, можно предсказывать направленность химических реакций и свойства соединений. Например, вещества, состоящие из элементов с большой разницей электроотрицательности, обычно обладают полярными химическими связями и имеют высокую растворимость в воде.
Основные свойства молекул
1. Размер и форма: Молекулы могут быть разных размеров и форм, в зависимости от количества и расположения атомов. Форма молекулы может влиять на ее свойства и способность взаимодействовать с другими веществами.
2. Валентность: Каждый атом в молекуле имеет свое количество валентных связей, то есть способность соединяться с другими атомами. Валентность атомов определяет тип и количество связей, которые они могут образовывать.
3. Полярность: Молекулы могут быть полярными или неполярными в зависимости от распределения зарядов внутри них. Полярные молекулы имеют разделенные электрические заряды и могут образовывать дипольные взаимодействия с другими молекулами, что влияет на их свойства.
4. Электроотрицательность: Электроотрицательность атома определяет его способность привлекать электроны в химической связи. Более электроотрицательные элементы в молекуле обычно имеют большую электронную плотность и могут сильнее притягивать электроны, что может влиять на химические реакции и свойства молекулы.
5. Масса: Масса молекулы определяет ее физические свойства, такие как плотность и температура плавления и кипения. Большие молекулы обычно имеют более высокую массу и могут обладать более сложными физическими свойствами.
Все эти свойства молекул играют важную роль в химических процессах и взаимодействии различных веществ.
Типичные химические элементы
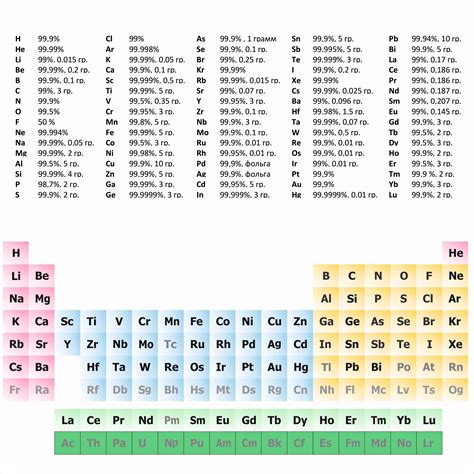
Металлы
- Железо (Fe)
- Алюминий (Al)
- Натрий (Na)
- Калий (K)
- Магний (Mg)
Металлы обладают хорошей электропроводностью и часто используются в промышленности для производства различных материалов и металлоконструкций.
Неметаллы
- Кислород (O)
- Углерод (C)
- Азот (N)
- Фосфор (P)
- Сера (S)
Неметаллы часто обладают низкой электропроводностью и могут быть газообразными при комнатной температуре. Они широко применяются в химической и фармацевтической промышленности.
Полуметаллы
- Германий (Ge)
- Селен (Se)
- Арсений (As)
- Бор (B)
- Теллур (Te)
Полуметаллы обладают промежуточными свойствами между металлами и неметаллами. Они используются в различных отраслях, включая электронику и соларные батареи.
Это лишь небольшая часть известных химических элементов. Каждый из них имеет свои уникальные свойства и применения, что делает их важными компонентами в практически всех сферах нашей жизни.
Атомное строение веществ
Атому ядро состоит из протонов, обладающих положительным зарядом, и нейтронов, не обладающих зарядом. Вокруг ядра расположены электроны, с отрицательным зарядом. Взаимодействие протонов и электронов обуславливает химические свойства атомов и их способность образовывать соединения.
Более электроотрицательный элемент в молекуле обладает большей силой притяжения электронной оболочки к себе, что приводит к поляризации молекулы. Это свойство имеет большое значение при реакциях обмена электронами, каталитических реакциях и других физических и химических процессах. Более электроотрицательные элементы часто привлекают электроны к себе и образуют ионный тип связи, в то время как менее электроотрицательные элементы предпочитают образовывать ковалентные связи.
| Элемент | Электроотрицательность |
|---|---|
| Фтор | 3.98 |
| Кислород | 3.44 |
| Азот | 3.04 |
| Углерод | 2.55 |
| Водород | 2.2 |
Как видно из таблицы, фтор является самым электроотрицательным элементом, а водород - наименее электроотрицательным. Относительные значения электроотрицательности элементов можно использовать для предсказания химических свойств веществ и определения типов химических связей между атомами.
Сравнение электроотрицательности

Для сравнения электроотрицательности атомов используется так называемая электроотрицательность Полинга. Эта шкала позволяет установить разницу в электроотрицательности между разными элементами.
Наиболее электроотрицательным элементом в периодической таблице является флуор. Он имеет самое высокое значение электроотрицательности - 4.0. Наоборот, самым электроотрицательным элементом считается франций, у которого значение электроотрицательности равно 0.7. На основе электроотрицательности атомов можно сделать вывод о типе химической связи, которая образуется между этими атомами.
Важно отметить, что электроотрицательность элемента может изменяться в зависимости от других атомов или групп атомов, с которыми он вступает в реакцию. Также, электроотрицательность может использоваться для определения полярности молекулы или соединения.
Физические и химические свойства
Более электроотрицательный элемент обладает особыми физическими и химическими свойствами, которые влияют на его реактивность и способность участвовать в различных химических реакциях.
Физические свойства более электроотрицательных элементов часто связаны с их атомной структурой. Эти элементы обычно имеют малую атомную радиус и высокую электронную плотность, что делает их склонными к притяжению электронов от других элементов. Они также имеют большую энергию ионизации - энергию, необходимую для удаления электрона из атома. Более электроотрицательные элементы обладают высокой электроотрицательностью, что указывает на их способность притягивать пары электронов в химических связях.
Химические свойства более электроотрицательного элемента определяют его реакционную способность и способность образовывать соединения с другими элементами. Эти элементы, как правило, формируют галогениды и оксиды с высокой степенью окисления. Более электроотрицательные элементы также проявляют высокую активность в реакциях с другими элементами, так как стремятся заполнить свою электронную оболочку и достичь стабильности.
Более электроотрицательные элементы также имеют способность образовывать полярные связи с менее электроотрицательными элементами. Это объясняет, почему более электроотрицательные элементы часто проявляют себя как электрофилы, притягивая электроны в химических реакциях. Более электроотрицательные элементы также могут образовывать ковалентные связи с другими электроотрицательными элементами, что приводит к образованию молекулярного соединения.








