Атомы - это основные строительные блоки вещества. Каждый химический элемент состоит из атомов одного вида. Значение атомов химического элемента заключается в их уникальных свойствах и способности образовывать связи с другими атомами.
Ключевым понятием в химии является атомный номер, который определяет порядковый номер элемента в таблице Менделеева. Атомный номер также указывает на количество протонов в ядре атома. Это число определяет химические свойства элемента и его положение в периодической системе элементов.
Электроны - это негативно заряженные частицы, которые обращаются вокруг ядра атома. Значение электронов заключается в их энергетических уровнях и возможности образования химических связей с другими атомами. Количество электронов в атоме определяется атомным номером и определяет внешнюю оболочку атома.
Основные свойства атомов, такие как масса, объем и плотность, определяются в основном их ядром. Протоны и нейтроны, составляющие ядро, имеют положительные заряды и вносят вклад в массу атома. Эти частицы также определяют стабильность и радиоактивность атомов.
Важно отметить, что химические свойства и поведение атомов одного элемента могут сильно различаться в зависимости от их количества, расположения и связи с другими атомами. Изучение атомов и их значений позволяет понять основные законы и принципы химии и обеспечивает основу для разработки новых материалов и технологий.
Атомы химического элемента: значимость и понятия
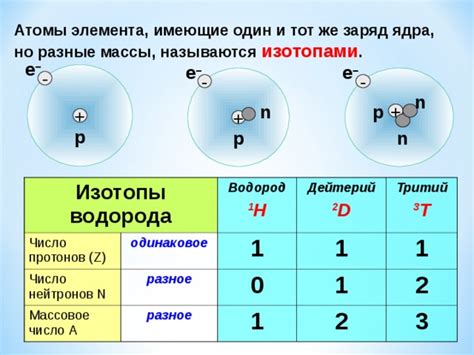
Атомы химических элементов характеризуются своим атомным номером, который определяет число протонов в ядре. Количество протонов и электронов в атоме, как правило, совпадает, что обеспечивает электрическую нейтральность атома.
Каждый химический элемент имеет свой уникальный атомный номер, а также символ, который изображается одной или двумя буквами латинского алфавита. Примеры таких символов: H для водорода, O для кислорода, Fe для железа.
Значимость атомов химических элементов заключается в их способности образовывать химические связи между собой. Атомы могут образовывать различные связи, такие как ионные, ковалентные или металлические. Эти связи определяют свойства вещества и его переходы между различными фазами.
| Элемент | Символ | Атомный номер |
|---|---|---|
| Водород | H | 1 |
| Кислород | O | 8 |
| Железо | Fe | 26 |
Через последние несколько столетий наши познания о структуре и свойствах атомов химических элементов значительно расширились, что позволяет нам лучше понять мир вокруг нас и использовать эти знания в различных областях, таких как химия, физика, биология и многое другое.
Определение и структура атома
Ядро атома содержит протоны и нейтроны. Протоны имеют положительный заряд, а нейтроны - не имеют заряда. Сумма протонов и нейтронов определяет массовое число атома.
Вокруг ядра атома находится электронная оболочка, состоящая из электронов. Электроны имеют отрицательный заряд и обладают массой, которая пренебрежимо мала по сравнению с массой протонов и нейтронов.
Внешняя оболочка - это самая дальняя от ядра оболочка, в которой находятся валентные электроны. Валентные электроны определяют химические свойства атома и его способность участвовать в химических реакциях.
Структура атома может быть изображена с помощью химической формулы, где символ элемента обозначает ядро атома, а индексы указывают количество протонов и нейтронов.
Электроны и их роль в атому
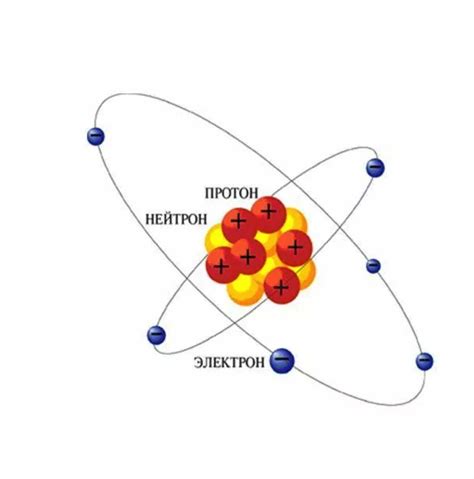
Атомы состоят из трех основных частиц: протонов, нейтронов и электронов. Электроны играют важную роль в атоме и определяют его характеристики и свойства.
- Электроны являются негативно заряженными элементарными частицами, находящимися вокруг ядра атома.
- Количество электронов в атому определяет его атомный номер и место в периодической таблице химических элементов.
- Электроны обладают массой, пренебрежимо малой по сравнению с протонами и нейтронами.
- Именно движение электронов вокруг ядра создает электронные облака, которые формируют нивелированный общий заряд атома.
- Возможность электронов занимать различные энергетические уровни в атоме определяет его валентность и возможность образования химических связей.
Таким образом, электроны являются ключевыми компонентами атома и имеют важное значение для его химических свойств и реактивности.
Ядро и протоны: основные характеристики
Протоны - это элементарные частицы с положительным электрическим зарядом, равным заряду электрона, но с противоположным знаком. Они являются стабильными и имеют массу, примерно в 1836 раз большую, чем масса электрона.
Основные характеристики протонов:
- Масса: примерно 1.67 x 10^-27 килограмма;
- Заряд: положительный элементарный заряд;
- Положение: находятся в ядре атома;
- Количество: число протонов в атомном ядре определяет химические свойства элемента и называется атомным номером.
Нейтроны и их влияние на свойства элемента

Число нейтронов в атоме определяет его массовое число. При добавлении или удалении нейтронов происходит образование изотопов – вариаций атома с различной массой. Некоторые изотопы могут быть стабильными, в то время как другие являются радиоактивными и подвергаются распаду со временем.
Наличие нейтронов в атоме влияет на его свойства. Чем больше массовое число атома, тем тяжелее он становится и, как правило, более устойчивым. Нейтроны также могут повлиять на ядерные реакции и способность вещества испускать или поглощать излучение.
Исследование влияния нейтронов на свойства элементов имеет важное значение в различных областях науки и технологий, включая ядерную физику, радиационную медицину, энергетику и материаловедение.
Взаимодействие атомов: реакции и связи
Атомы одного и того же химического элемента могут взаимодействовать друг с другом, образуя различные химические соединения. Взаимодействие атомов происходит в результате обмена или совместного использования электронов.
Наиболее распространенной формой взаимодействия атомов является химическая связь. Химическая связь возникает, когда атомы обмениваются электронами, чтобы достичь электронной конфигурации благородного газа, а именно восьми электронов в внешней оболочке. Через химическую связь образуются молекулы и кристаллические решетки, в которых атомы расположены в определенном порядке.
Если атомы разных элементов объединяются друг с другом, образуется химическое соединение. Частицы, образующие химическое соединение, называются молекулами. В молекулах атомы могут быть связаны разными типами связей, такими как ионная связь, ковалентная связь или металлическая связь.
Кроме того, атомы могут участвовать в химических реакциях, в результате которых происходят перестройки внутренней структуры атомов и образуются новые соединения. Химические реакции могут протекать с участием одного или нескольких элементов, в зависимости от типа взаимодействия.
Знание взаимодействия атомов позволяет понять химические свойства и реактивность различных элементов. Это имеет важное значение для разработки новых материалов, лекарственных препаратов, пищевых добавок и многих других продуктов.
| Тип связи | Описание |
|---|---|
| Ионная связь | Возникает при передаче электронов от одного атома к другому, образуя положительно и отрицательно заряженные ионы. |
| Ковалентная связь | Возникает при совместном использовании электронов двумя или более атомами. |
| Металлическая связь | Возникает между атомами металлов, когда их внешние электроны свободно движутся вокруг положительно заряженного ядра. |








