Анод и катод – это два основных понятия, которые широко используются в электрохимии и электронике. Эти термины обозначают электроды, играющие важную роль в различных процессах, связанных с перемещением зарядов. Понимание анода и катода является основой для понимания работы батарей, электролитических ячеек, электролиза и других электрохимических процессов.
Анод – это положительно заряженный электрод, на который переносятся отрицательно заряженные ионы, электроны или электромагнитные волны. В электрохимических процессах, анод отрицательно заряжается относительно катода и окисляется, теряя электроны. Анодом также называется электрод в батарее или аккумуляторе, откуда ток поступает во внешнюю цепь. Анод в электронном приборе является точкой подключения питания, откуда ток распространяется по различным элементам системы.
Например, в электролизе воды анодом является положительно заряженный электрод, на котором происходит окисление воды, а катодом – отрицательно заряженный электрод, на котором происходит восстановление воды. Это приводит к разложению воды на кислород и водород.
Катод – это отрицательно заряженный электрод, который принимает перенесенные на него положительно заряженные ионы, электроны или электромагнитные волны. В электрохимических процессах, катод положительно заряжается относительно анода и происходит снижение его заряда. В электронных устройствах, катод – это точка подключения, где ток покидает систему или устройство. В лампочке катод - это нить, на которую сходятся электроны и которая нагревается до свечения.
Анод и катод: основные понятия
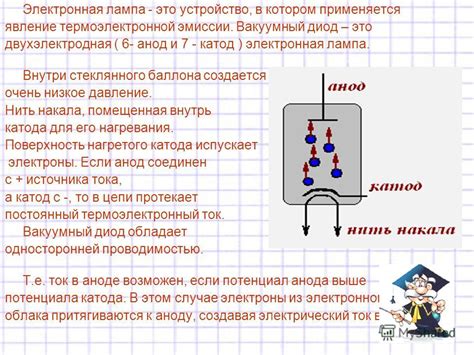
Анод - это положительно заряженный электрод, на котором происходит окисление или потеря электронов. В электрохимических процессах анод притягивает анионы, что способствует их окислению. В электротехнике анод - это терминал или контакт, через который вводится положительное напряжение в устройство.
Катод - это отрицательно заряженный электрод, на котором происходит восстановление или приобретение электронов. В электрохимических процессах катод притягивает катионы, что способствует их восстановлению. В электротехнике катод - это терминал или контакт, через который выводится отрицательное напряжение из устройства.
Разница потенциалов между анодом и катодом создает электрическую силу, которая позволяет электрона
Что такое анод?
В гальваническом элементе анод - это полюс, с которого ток вытекает из внешней цепи, а в электролизере анод выполняет роль электрода, на котором происходит окисление реагента.
Анод также может использоваться в качестве положительного электрода в электронных устройствах, таких как лампы или диоды, где он отвечает за приток электронов.
Примеры анода включают в себя аноды в автомобильных аккумуляторах, аноды водородных топливных элементов и аноды в гальванических элементах, таких как цинк-углеродные или алкалиновые батареи.
Что такое катод?
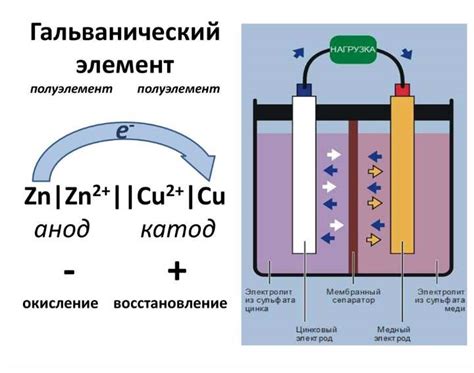
Катод обычно обозначается отрицательным знаком "-" в электрических схемах и электронных устройствах. При подаче электрического тока на катод, он притягивает электроны, которые двигаются от анода (положительного электрода) к катоду.
Катоды могут быть изготовлены из различных материалов, таких как металлы, полупроводники или смеси веществ. Например, катодами в электрических лампах служат тонкие проволочки или покрытия из никеля или вольфрама.
В электролитической ячейке, которая используется для хранения энергии, один из электродов является катодом. Катод в такой ячейке принимает электроны, которые заряжают активные материалы ячейки, такие как металлы или полупроводники.
В целом, катод играет важную роль в электронике и электрохимии, предоставляя место для прохождения электронов в электрической цепи и включаясь в различные технологии и устройства.
Как работают анод и катод в электрохимической ячейке?
Анод - это положительно заряженный электрод, на котором происходит окисление вещества. Во время окисления анода, электроны отдаются во внешнюю цепь, а положительные ионы перемещаются через электролит. Примером анода может служить сплав цинка или углеродный стержень, обычно с включением других материалов.
Катод - это отрицательно заряженный электрод, на котором происходит восстановление вещества. Во время восстановления катода, электроны из внешней цепи поступают на катод, а отрицательные ионы перемещаются через электролит. Примером катода может служить медный стержень, покрытый медью или другим металлом.
Работа анода и катода в электрохимической ячейке основана на разности потенциалов между ними. Эта разность приводит к возникновению электромоторной силы (ЭМС), которая вызывает движение электронов по внешней цепи и ионов через электролит. Таким образом, энергия химической реакции превращается в электрическую энергию, которая может быть использована для питания устройств.
Примеры использования анода и катода в быту и промышленности
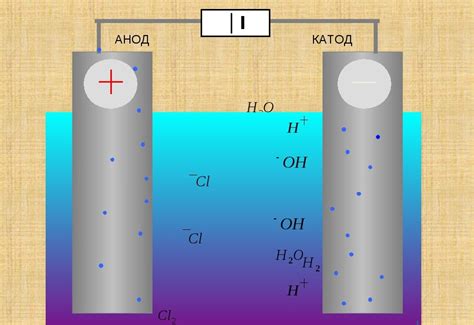
Аноды и катоды широко используются в различных сферах быта и промышленности. Вот несколько примеров их применения:
Бытовая электроника: Аноды и катоды используются в различных электронных устройствах, таких как телевизоры, компьютеры и мобильные телефоны. Аноды отвечают за выпуск электронов, а катоды за их прием и обработку.
Аккумуляторы: Аноды и катоды являются основными компонентами аккумуляторов. Аноды служат для окисления химических веществ, а катоды для восстановления. Это позволяет аккумуляторам сохранять и выделять энергию.
Электролиз: Аноды и катоды применяются в процессе электролиза для разделения различных веществ на составные части. Например, в производстве алюминия анодом служит углеродная пластина, а катодом - покрытый алюминием стержень.
Защита от коррозии: Аноды используются для защиты различных металлических конструкций от коррозии. В таких случаях анод выполняет функцию жертвенного металла, притягивая коррозионные процессы на себя и предотвращая повреждения основного металла.
Медицинская техника: Аноды и катоды применяются в медицинской технике, например, для гальванического разложения воды при получении кислорода и водорода.
Электрохимические процессы: Аноды и катоды используются в различных электрохимических процессах, таких как электрохимическая очистка воды и электроосаждение металлов на поверхности изделий.
Это лишь некоторые примеры использования анода и катода в быту и промышленности. Их роль и значение трудно переоценить, так как они играют важную роль в самых разных областях нашей жизни.
Анод и катод в батареях
В простейших типах батарей, таких как щелочные или цинковые батареи, анодом обычно является металлический мешок, заполненный окислительной пастой. Щелочной или цинковый оболочка служит как катод, а серная паста между ними действует как электролит.
В процессе разрядки батареи, окислитель в пасте анода начинает разлагаться, отдавая электроны на анод. Затем электроны движутся через внешнюю цепь от анода к катоду, где происходит восстановление окислителя и формирование стабильного электролитического баланса. Таким образом, анод и катод играют важную роль в поддержании электрического тока в батареях.
| Тип батареи | Анод | Катод |
|---|---|---|
| Щелочная батарея | Металлический мешок, заполненный окислительной пастой | Цинковый оболочка |
| Цинковая батарея | Цинковый оболочка | Медный стержень |
Анод и катод в гальванизации
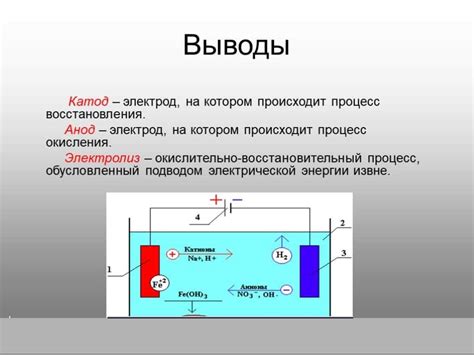
Анод – это положительно заряженный электрод, который служит источником положительных ионов металла, который будет нанесен на поверхность. В гальванизации анод изготавливают из материала, который соответствует металлу, который планируется нанести на поверхность. Например, при гальванизации железа анодом может быть кусок чистого железа.
Катод – это отрицательно заряженный электрод, на который будут осаждаться положительные ионы металла. Катод изготавливают из материала, на который будет нанесено покрытие. Например, при гальванизации железа, катодом может быть заготовка из стали, которую нужно покрыть слоем никеля.
В ходе гальванизации между анодом и катодом создается электрическое поле, которое позволяет металлу осаждаться равномерно на поверхности катода. Таким образом, гальваническое покрытие придает предмету устойчивость к коррозии, а также может изменить его внешний вид и свойства.
У анода и катода есть свои особенности и роли, их выбор влияет на качество и характеристики гальванического покрытия. Правильный выбор материалов для анода и катода – важный шаг в процессе гальванизации.
Анод и катод в электролизе
В процессе электролиза, анод и катод соединяются с источником постоянного тока и погружаются в электролит – вещество, которое разлагается на положительные и отрицательные ионы. Положительные ионы будут двигаться к катоду, а отрицательные – к аноду.
На аноде происходит окисление ионов, в результате которого образуются электроны и нейтральные атомы. Эти электроны затем перемещаются к катоду через проводник и участвуют в реакции восстановления. На катоде происходит процесс восстановления, при котором электроны принимаются восстанавливающими ионами, образуя новые соединения.
С помощью анода и катода можно осуществлять различные процессы электролиза. Например, в процессе электролиза растворов меди (II) сульфата, на аноде происходит окисление меди и образование иона меди (II), а на катоде происходит восстановление иона меди (II) до нейтрального атома меди.
Таким образом, анод и катод в электролизе играют важную роль в процессе распада и восстановления соединений под воздействием электрического тока.








