Насыщенные растворы являются одной из основных концепций химии. Они обладают важным значением в различных химических реакциях и процессах. Насыщенный раствор можно определить как раствор, в котором количество растворенного вещества достигает максимального возможного значения при заданной температуре и давлении.
В основе понятия насыщенных растворов лежит равновесие между процессом растворения и обратным процессом кристаллизации или осаждения вещества. В насыщенном растворе скорость растворения равна скорости осаждения, что приводит к динамическому равновесию.
Важно отметить, что насыщенные растворы имеют определенное значение в химических реакциях. Они могут способствовать как ускорению, так и замедлению процессов реакции в зависимости от конкретных условий и химического взаимодействия.
Например, в реакции образования кристаллов из раствора, насыщенный раствор может способствовать образованию осадка, поскольку достигнута максимальная концентрация растворенного вещества. С другой стороны, в реакции растворения, насыщенный раствор может замедлить процесс, поскольку больше вещества уже не может быть распределено в растворе.
Таким образом, понимание значения насыщенных растворов и их влияния на химические реакции помогает лучше понять и контролировать реакционные процессы в химии.
Значение насыщенных растворов
Основное значение насыщенных растворов заключается в их использовании в качестве исходных веществ для проведения различных химических реакций. Насыщенные растворы часто используются в лабораторных и промышленных условиях для получения новых соединений и материалов.
Кроме того, насыщенные растворы используются в процессе выделения и очистки веществ. Они позволяют разделить смешанные вещества и удалить нежелательные примеси.
В некоторых случаях насыщенные растворы могут играть важную роль в биологических системах. Например, в организме человека насыщенные растворы играют важную роль в процессе переваривания пищи и обмена веществ.
Насыщенные растворы также имеют значение в проведении экспериментов и исследований. Их свойства и поведение могут быть изучены для получения новых знаний о растворимости веществ и химических процессах.
Реакции в насыщенных растворах
В насыщенных растворах могут происходить химические реакции между растворенным веществом и другими реагентами, находящимися в растворителе. Эти реакции могут протекать быстрее или медленнее, чем в чистом растворе, и могут меняться в зависимости от концентрации растворенного вещества.
Влияние насыщенных растворов на химические реакции может проявляться в различных аспектах. Например, концентрация растворенного вещества может влиять на скорость реакции или на направление процесса. Насыщенные растворы могут также участвовать в каталитических реакциях и способствовать их протеканию.
Важно отметить, что состав и характер насыщенных растворов могут быть разными. Они могут быть насыщенными растворами солей, кислот, оснований, органических соединений и других веществ. Все эти растворы имеют свои специфические свойства и необходимо учитывать их влияние на химические реакции, происходящие в них.
- Насыщенные растворы солей могут обладать особенной электролитической активностью и способностью участвовать в реакциях с другими электролитами.
- Насыщенные растворы кислот и оснований могут образовывать ионы, которые влияют на pH раствора и способность других реагентов протекать в растворе.
- Насыщенные растворы органических соединений могут обладать способностью участвовать в реакциях с другими органическими соединениями и изменять конформацию молекул.
Исследование реакций, происходящих в насыщенных растворах, позволяет лучше понять особенности взаимодействия веществ и их влияние на окружающую среду. Это является важным аспектом в различных областях науки, таких как химия, фармацевтика, пищевая промышленность и др.
Правило насыщенности

Согласно правилу насыщенности, если растворить большее количество вещества, чем максимально возможное при заданных условиях, то оно останется нерастворенным на дне сосуда или выпадет в форме осадка. Такой раствор называется насыщенным.
Значение насыщенных растворов и их влияние на химические реакции заключаются в том, что они являются основой для проведения множества экспериментов и реакций.
Насыщенные растворы используются для определения концентрации вещества, проведения химических реакций с участием вещества, изучения свойств растворов и проведения различных аналитических методов анализа.
Применение насыщенных растворов позволяет получить более точные и надежные результаты в химических исследованиях. Они также являются важным инструментом для многих отраслей науки и техники, в том числе фармацевтики, пищевой промышленности и технологии, аналитической химии и др.
Концентрация растворов и химические реакции
На химические реакции влияет как абсолютная концентрация раствора, так и относительная концентрация растворимых компонентов. Повышение концентрации раствора может ускорить химическую реакцию, так как увеличивается количество частиц, способных вступить в реакцию.
Насыщенные растворы, в которых достигнута максимальная концентрация растворенного вещества при данной температуре, также оказывают влияние на процесс химической реакции. Если реакция требует растворенного вещества, но его концентрация в насыщенном растворе достигает предела, то скорость реакции может замедляться или вообще прекращаться.
Кроме того, концентрация раствора может влиять на равновесие некоторых химических реакций. По принципу Ле-Шателье, повышение концентрации одного из реагентов приведет к смещению равновесия в сторону образования продукта реакции с меньшей концентрацией.
Таким образом, концентрация растворов является важным фактором, влияющим на химические реакции. Она определяет скорость реакции, эффективность протекания реакции и равновесие системы.
Эффект насыщенности на скорость реакций

Насыщенные растворы играют важную роль в химических реакциях, так как они могут оказывать значительное влияние на их скорость. Насыщенное состояние раствора достигается, когда его концентрация становится максимальной при определенной температуре.
Когда раствор становится насыщенным, его молекулы или ионы распределяются равномерно во всем объеме раствора, и в этом состоянии их концентрация остается постоянной. В таком состоянии раствор не может вмещать больше растворенных веществ, и любые добавления к насыщенному раствору будут оставаться нерастворимыми или образовывать осадок.
Когда исследователям нужно провести реакцию в насыщенном растворе, они могут увидеть, что скорость реакции становится медленнее по сравнению с реакцией в более разбавленном растворе. Этот эффект насыщенности обусловлен наличием большого количества растворенных частиц, которые препятствуют диффузии или столкновению молекул реагента в должном объеме.
Однако насыщение может также способствовать увеличению скорости реакции. В случае экзотермической реакции, насыщенные растворы могут обеспечить более высокую температуру реакции, что приводит к ускорению скорости. Также в некоторых случаях насыщенные растворы могут работать как буферные системы, изменяя pH среды и, тем самым, влияя на химическую реакцию.
- Скорость реакции может быть как увеличена, так и уменьшена насыщением раствора.
- Насыщенные растворы не могут вмещать больше растворенных веществ.
- Диффузия и столкновение молекул реагента могут быть затруднены в насыщенных растворах.
- Насыщенные растворы могут повысить температуру реакции или изменить pH раствора, что может влиять на скорость реакции.
Исследование и понимание эффекта насыщенности на скорость реакций являются важными аспектами химических наук и могут иметь влияние на различные области исследований, а также на промышленность и технологии.
Влияние насыщенных растворов на химические реакции
Насыщенные растворы играют важную роль в химических реакциях. Они обладают способностью изменять ход и скорость химических превращений.
Один из основных эффектов насыщенного раствора - изменение равновесия химической реакции. Раствор может изменить концентрацию реагентов и продуктов, что в свою очередь сказывается на положении равновесия реакции. Насыщенный раствор может сдвинуть равновесие в одну или другую сторону, что приведет к увеличению или уменьшению концентрации определенного вещества.
Другим важным аспектом влияния насыщенного раствора на реакции является его влияние на кинетику реакции - скорость протекания химической реакции. Насыщенный раствор может либо ускорить, либо замедлить химическую реакцию в зависимости от характера реагентов и условий проведения реакции.
Влияние насыщенных растворов на реакции может быть использовано в различных областях, включая синтез новых веществ, определение концентраций и исследование кинетических характеристик реакций. Анализ и учет влияния насыщенных растворов на химические реакции позволяют получать более точные результаты и предсказывать их характеристики.
Изменение скорости реакций

Один из факторов, который может значительно влиять на скорость реакции, - это насыщенность раствора. В насыщенном растворе концентрация растворенного вещества находится на пределе растворимости для данной температуры. Это означает, что больше вещество не может раствориться и сохраняется равновесие между растворенным и нерастворенным веществом.
На скорость реакции может оказывать влияние насыщенность раствора через так называемый "эффект супернасыщения". Когда реагенты в насыщенном растворе находятся в более высокой концентрации, чем было бы возможно при равновесии, скорость реакции может увеличиваться. Это происходит потому, что реагенты могут сталкиваться чаще и с большей энергией, что способствует более частым и успешным реакциям.
С другой стороны, насыщенные растворы могут также замедлять скорость реакции. Это может происходить, когда насыщенный раствор является продуктом реакции и может вызывать обратную реакцию. При этом обратная реакция может происходить в более медленном темпе, чем прямая реакция, что приводит к замедлению реакции в целом.
Влияние насыщенных растворов на скорость реакции может быть значительным и может играть важную роль в различных химических процессах и промышленных процессах. Понимание этого влияния может помочь в оптимизации реакций и улучшении эффективности процессов.
Влияние на равновесие реакций
Свойства насыщенных растворов могут влиять на равновесие химических реакций. Концентрация и химическая активность растворенных веществ могут оказывать значительное влияние на направление и скорость реакции. Это связано с принципами Ле-Шателье и массовым действием.
Принцип Ле-Шателье утверждает, что если на химическую систему, находящуюся в равновесии, оказывается внешнее воздействие (изменение концентрации реагентов или продуктов, температуры и давления), система смещается в направлении, которое компенсирует это изменение и восстанавливает равновесие. Например, если в раствор добавить некоторое количество реагента, равновесная система будет смещаться в направлении реакции, уменьшающей концентрацию этого реагента.
Массовое действие объясняет, как концентрация реагентов и продуктов влияет на скорость реакции. Когда концентрация реагентов высока, вероятность коллизий и, следовательно, скорость реакции увеличиваются. Поэтому, при добавлении реагента в насыщенный раствор, скорость соответствующей реакции может возрасти.
Таким образом, насыщенные растворы могут влиять на равновесие реакций путем изменения концентрации веществ и их химической активности. Это явление имеет важное значение в химии и может использоваться для контроля направления и скорости реакций в различных процессах и промышленных производствах.
Примеры химических реакций в насыщенных растворах
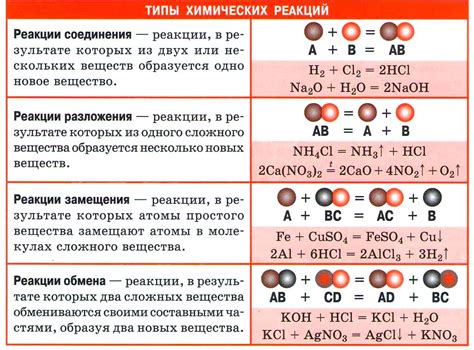
Насыщенные растворы играют важную роль в различных химических реакциях. В них могут происходить различные процессы, включая образование новых веществ, проявление химических свойств соединений, обмен ионами и т.д. В данном разделе рассмотрим несколько примеров химических реакций, которые могут происходить в насыщенных растворах.
Нейтрализационная реакция: кислота + щелочь → соль + вода. Примером такой реакции является реакция между соляной кислотой (HCl) и гидроксидом натрия (NaOH). При смешивании этих реактивов в насыщенном растворе образуется соль - хлорид натрия (NaCl) и вода (H2O).
Окислительно-восстановительная реакция: окислитель + вещество для восстановления → окисленное вещество + восстановленное вещество. Примером такой реакции является реакция между хлором (Cl2) и йодидом калия (KI) в насыщенном растворе. При смешивании этих реагентов образуются окисленное вещество - йод (I2) и восстановленное вещество - хлорид калия (KCl).
Процесс обмена ионами: ион из одного раствора замещается ионом из другого раствора. Примером такого процесса является реакция между нитратом серебра (AgNO3) и хлоридом натрия (NaCl) в насыщенном растворе. При смешивании этих реагентов образуется осадок - хлорид серебра (AgCl), тогда как нитрат натрия (NaNO3) остается в растворе.
Это лишь несколько примеров химических реакций, которые могут происходить в насыщенных растворах. В зависимости от соединений, условий реакции и множества других факторов, реакции в насыщенных растворах могут быть очень разнообразными и иметь различные характеристики.








