Молекулярный вид реакций - это концепция химических реакций, которая основывается на представлении реакций как взаимодействия отдельных молекул. В этой концепции реакции протекают на молекулярном уровне, где каждая молекула играет определенную роль и претерпевает изменения.
Преимущество молекулярного вида реакций заключается в его способности объяснить механизмы и кинетику реакций. Он позволяет понять, как именно различные молекулы взаимодействуют между собой и какие образуются новые соединения. Также молекулярный вид реакций помогает предсказывать и объяснять реакционные условия, стереохимию и разные пути протекания реакций.
Для лучшего понимания молекулярного вида реакций можно рассмотреть пример. Например, реакцию гидролиза эфира в кислой среде. В этой реакции молекула эфира взаимодействует с молекулой воды, протекает обмен протонов и образуются две новые молекулы: алкоголь и кислота. Молекулярный вид этой реакции позволяет увидеть каждый из этих этапов и понять, как именно происходит превращение эфира в алкоголь и кислоту.
Молекулярный вид реакций: основное понятие
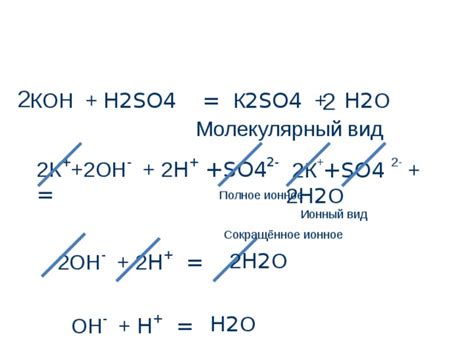
Молекулярный вид реакций основывается на представлении реакций в виде химических уравнений, где каждая молекула выступает как отдельный участник реакции. Например, при реакции сжигания метана (CH4) с кислородом (O2) образуются углекислый газ (CO2) и вода (H2O):
CH4 + 2O2 → CO2 + 2H2O
Согласно молекулярному виду реакций, каждая молекула метана и кислорода сталкиваются между собой и переходят в новые молекулы, а именно молекулы углекислого газа и воды.
Молекулярный вид реакций позволяет исследовать и предсказывать результаты различных химических реакций, а также проводить расчеты, связанные с количественными изменениями вещества в процессе реакции.
Что такое молекулярный вид реакций
В молекулярном виде реакций используются химические уравнения для представления реакций между молекулами. В уравнениях отображаются реагенты, продукты и коэффициенты, которые показывают соотношение между молекулами.
Пример молекулярного вида реакции:
- Реакция: H2 + Cl2 → 2HCl
- Молекулярный вид: H2 + Cl2 → 2HCl
В этом примере, две молекулы водорода (H2) реагируют с двумя молекулами хлора (Cl2), образуя две молекулы соляной кислоты (HCl).
Молекулярный вид реакций позволяет химикам понять, какие молекулы участвуют в реакции и какие молекулы образуются в результате. Это важно для понимания химических процессов и разработки новых соединений и материалов.
Принципы молекулярного вида реакций
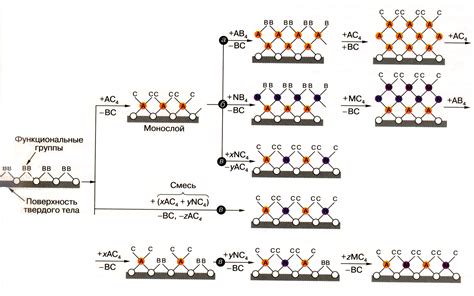
Основные принципы молекулярного вида реакций:
- Реакции происходят между отдельными молекулами вещества. Каждая молекула может быть вовлечена в реакцию независимо от других молекул того же вещества.
- Молекулы вещества объединяются и распадаются узлами активации реакции.
- При реакции между молекулами возникают новые химические связи, а также формируются или разрушаются функциональные группы.
- Каждый шаг реакции является элементарным актом, то есть имеет свою специфичную скорость и молекулярную структуру.
- Общая реакция является суммой всех элементарных актов, происходящих последовательно или параллельно.
- Поскольку реакции происходят между отдельными молекулами, их вероятность зависит от концентрации реагентов и температуры.
Примеры реакций, объясняемых молекулярным видом:
- Горение: молекулы горючего вещества (например, метана) соприкасаются с молекулами кислорода и образуют продукты горения (например, воду и углекислый газ).
- Растворение: молекулы растворяемого вещества взаимодействуют с молекулами растворителя и образуют раствор.
- Гидролиз: молекулы вещества разрушаются в результате реакции с молекулами воды.
- Окислительно-восстановительные реакции: молекулы окислителя и восстановителя взаимодействуют, образуя окисленную и восстановленную формы вещества.
Использование молекулярного вида реакций позволяет более подробно и точно описывать происходящие процессы и предсказывать их результаты в химической реакции.
Объяснение молекулярного вида реакций
Этот подход основывается на представлении о том, что химические реакции происходят на уровне молекулярных взаимодействий. Каждая молекула вещества взаимодействует с другими молекулами, образуя новые химические связи или разрушая существующие. В результате таких взаимодействий происходит химическая реакция.
Пример молекулярной реакции - реакция между молекулами воды и молекулами соли:
2H2O(l) + NaCl(s) → 2H2O(l) + NaCl(aq)
В этой реакции две молекулы воды и одна молекула соли взаимодействуют друг с другом, образуя две молекулы воды и раствор соли. Видно, что реакция происходит на молекулярном уровне, с участием конкретных молекул вещества.
Этот подход к объяснению реакций позволяет более детально изучать протекающие процессы, а также предсказывать результаты реакций и разрабатывать новые химические соединения и материалы.
Примеры молекулярного вида реакций
Пример 1:
Реакция синтеза воды:
2H2 + O2 → 2H2O
В этой реакции две молекулы водорода (H2) и одна молекула кислорода (O2) соединяются между собой, образуя две молекулы воды (H2O).
Пример 2:
Реакция разложения аммиака:
2NH3 → N2 + 3H2
В этой реакции две молекулы аммиака (NH3) разлагаются на молекулу азота (N2) и три молекулы водорода (H2).
Пример 3:
Реакция сгорания метана:
CH4 + 2O2 → CO2 + 2H2O
В этой реакции молекула метана (CH4) реагирует с двумя молекулами кислорода (O2), образуя молекулу углекислого газа (CO2) и две молекулы воды (H2O).
Это лишь некоторые примеры молекулярного вида реакций, которые помогают увидеть и понять, какие молекулы участвуют в химических процессах и как они преобразуются друг в друга.








