Массовая доля раствора - это величина, которая показывает, сколько массы растворенного вещества содержится в определенном объеме раствора. Она выражается в процентах и является одной из основных характеристик раствора.
Массовая доля раствора рассчитывается путем деления массы растворенного вещества на общую массу раствора и умножения полученного значения на 100%. Таким образом, можно определить, насколько раствор насыщен определенным веществом и какое количество данного вещества находится в растворе.
Например, если в 100 граммах раствора содержится 20 граммов соли, то массовая доля раствора соли будет равна 20%.
Массовая доля раствора является важной характеристикой в химии и используется для описания различных химических процессов и реакций. Она позволяет определить концентрацию вещества в растворе и проводить расчеты при проведении химических экспериментов.
Что такое массовая доля раствора?

Массовая доля раствора является одним из способов измерения концентрации растворов. Она позволяет определить, насколько раствор является концентрированным или разбавленным. Чем выше массовая доля раствора, тем больше растворенного вещества содержится в данном растворе.
Для определения массовой доли раствора необходимо знать массу растворенного вещества и массу всего раствора. Формула для расчета массовой доли раствора выглядит следующим образом:
Массовая доля раствора = (масса растворенного вещества / масса всего раствора) × 100%
Например, если у нас имеется 200 г раствора, в котором растворено 20 г соли, то массовая доля раствора будет равна:
Массовая доля раствора = (20 г / 200 г) × 100% = 10%
Таким образом, в данном примере массовая доля раствора составляет 10%, что означает, что 10% массы всего раствора приходится на массу соли.
Массовая доля раствора имеет важное значение в химии и применяется для определения концентрации различных растворов. Зная массовую долю раствора, можно регулировать и контролировать процессы растворения и использования веществ в различных отраслях науки и промышленности.
Определение массовой доли
Массовую долю обычно обозначают символом w, а иногда также используют символы m или М (от английского слова "mass").
Массовая доля может быть вычислена по формуле:
w = (mвещества / mсмеси) × 100%
где:
- w – массовая доля вещества;
- mвещества – масса вещества;
- mсмеси – общая масса смеси.
Пример:
| Вещество | Масса, г | Массовая доля, % |
|---|---|---|
| Вода (H2O) | 90 | 90% |
| Соль (NaCl) | 10 | 10% |
| Общая масса | 100 | - |
Формула для расчета массовой доли

массовая доля (м) = (масса растворенного вещества / общая масса раствора) * 100%
где:
- масса растворенного вещества - масса вещества, которое было растворено;
- общая масса раствора - сумма массы растворенного вещества и массы растворителя (обычно вода).
Формула позволяет выразить массовую долю в процентах, что удобно для определения концентрации раствора.
Пример: если в 100 г раствора содержится 20 г растворенного вещества, то массовая доля будет равна:
массовая доля = (20 г / 100 г) * 100% = 20%.
Примеры расчета массовой доли
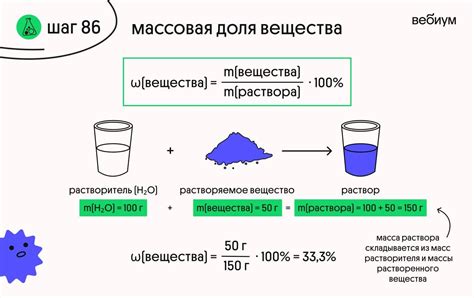
Пример 1: Рассмотрим раствор, содержащий 50 г сахара и 150 г воды. Чтобы определить массовую долю сахара в этом растворе, мы должны разделить массу сахара на общую массу раствора и умножить результат на 100%:
Массовая доля сахара = (50 г / (50 г + 150 г)) × 100% = 25%.
Пример 2: Рассмотрим раствор, содержащий 30 мл спирта и 70 мл воды. Чтобы определить массовую долю спирта в этом растворе, мы должны знать плотность спирта и плотность воды. Предположим, что плотность спирта равна 0.789 г/мл, а плотность воды равна 1 г/мл. Тогда мы можем расчитать массу каждого компонента:
Масса спирта = 30 мл × 0.789 г/мл = 23.67 г.
Масса воды = 70 мл × 1 г/мл = 70 г.
Общая масса раствора = Масса спирта + Масса воды = 23.67 г + 70 г = 93.67 г.
Массовая доля спирта = (23.67 г / 93.67 г) × 100% ≈ 25.27%.
Пример 3: Рассмотрим смесь соли, содержащую 40 г натрия и 60 г калия. Чтобы определить массовую долю натрия в этой смеси, мы должны разделить массу натрия на общую массу смеси и умножить результат на 100%:
Массовая доля натрия = (40 г / (40 г + 60 г)) × 100% = 40%.
Это всего лишь несколько примеров расчета массовой доли, и в каждом конкретном случае могут быть использованы различные формулы или методы расчета в зависимости от характеристик раствора или смеси. Определение массовой доли позволяет более точно описывать состав вещества и проводить различные аналитические исследования.
Значение массовой доли в химии

Массовая доля выражается в процентах и рассчитывается следующим образом:
Массовая доля (%) = (масса вещества / масса раствора) * 100%
Например, если у нас есть раствор с массой 100 г, в котором содержится 20 г соли, то массовая доля соли в этом растворе будет:
Массовая доля (%) = (20 г / 100 г) * 100% = 20%
Таким образом, массовая доля позволяет определить, насколько концентрированным является раствор и какое количество вещества содержится в нем. Это особенно важно для проведения химических реакций и контроля качества веществ, а также для выполнения точных экспериментов и расчетов.
Влияние массовой доли на свойства растворов
Массовая доля имеет прямое влияние на физические и химические свойства раствора. Например, массовая доля вещества может определять его растворимость или скорость реакции. В растворах с высокой массовой долей вещества, реакция может протекать более интенсивно, так как большое количество вещества влечет за собой большее количество возможных взаимодействий.
Также массовая доля может влиять на физические свойства раствора, такие как плотность, вязкость и поверхностное натяжение. Например, раствор с высокой массовой долей растворимого вещества может иметь большую плотность, чем раствор с низкой массовой долей.
Определение и контроль массовой доли раствора играют важную роль в различных областях, таких как химия, фармацевтика, пищевая промышленность и т.д. Точное знание массовой доли позволяет правильно расчитывать и контролировать процессы, оптимизировать условия и достичь желаемых свойств раствора.
Массовая доля раствора в медицине
Медицинские растворы, включая инфузионные и пищевые растворы, содержат различные вещества, такие как лекарственные препараты, витамины, минералы и другие полезные соединения. Знание массовой доли раствора в медицине позволяет врачам и фармацевтам точно рассчитать дозировку и определить необходимое количество вещества, которое должно быть введено пациенту.
| Примеры препаратов | Массовая доля раствора |
|---|---|
| Калия хлорид | 10% |
| Натрия хлорид | 0.9% |
| Декстроза | 5% |
| Кальция глюконат | 10% |
В рецептах медицинских препаратов указывается массовая доля раствора, чтобы ясно указать, сколько граммов активного вещества должно быть добавлено к определенному объему раствора. Такие препараты часто используются для внутривенного, опорного или местного применения, и точное соотношение массовой доли раствора очень важно для обеспечения правильной терапевтической дозы.
Как измерить массовую долю раствора?
Для измерения массовой доли раствора важно знать массу растворимого вещества и массу всего раствора.
Для начала нужно взвесить сухое растворимое вещество. Масса растворимого вещества обычно измеряется в граммах на аналитических весах с точностью до сотых или тысячных долей грамма.
Затем необходимо измерить массу всего раствора. Это можно сделать, например, с помощью градуированной колбы или мерного цилиндра. Нужно помнить, что при измерении массы раствора следует учитывать массу и самого сосуда.
Чтобы определить массовую долю раствора, необходимо разделить массу растворимого вещества на массу всего раствора и умножить результат на 100%. Таким образом получится процентное значение массовой доли раствора.
Например, если масса растворимого вещества равна 20 г, а масса всего раствора – 100 г, то массовая доля раствора составит 20%.








