Газовая постоянная является одним из самых фундаментальных понятий в физике и химии. Этот термин используется для обозначения величины, характеризующей поведение газов при изменении условий. Газовая постоянная обозначается символом R и имеет значение, которое отличается, в зависимости от используемой единицы измерения.
Наиболее известной формой уравнения, в котором фигурирует газовая постоянная, является уравнение состояния идеального газа. Оно гласит: PV = nRT, где P - давление газа, V - его объем, n - количество вещества, T - температура в абсолютной шкале, а R - газовая постоянная.
Газовая постоянная является универсальной константой, которая позволяет связать между собой объем, давление, количество вещества и температуру газового состояния в рамках идеальной модели. Это означает, что при сохранении других условий, как только один из параметров изменяется, остальные тоже меняются пропорционально, и их связь задается газовой постоянной.
В различных системах единиц, значения газовой постоянной могут различаться. Наиболее распространенными являются такие значения, как 8,314 Дж/(моль·К) и 0,0821 атм·л/(моль·К). Газовая постоянная используется для решения множества физических и химических задач, связанных с поведением газов, и является одним из ключевых понятий, необходимых для понимания многих явлений и процессов в природе и технике.
Газовая постоянная: основные понятия

Основными понятиями, связанными с газовой постоянной, являются:
- Идеальный газ - это модель газа, в которой предполагается, что межмолекулярные взаимодействия отсутствуют, а молекулы движутся без каких-либо ограничений. Эта модель хорошо описывает поведение газов при низких давлениях и высоких температурах.
- Давление - это сила, действующая на единицу площади. Давление газа зависит от числа и силы столкновений молекул газа со стенками сосуда, в котором он находится.
- Объем - это количество пространства, занимаемое газом. Объем газа может изменяться при изменении давления и/или температуры.
- Температура - это мера теплового движения молекул газа. Чем выше температура, тем быстрее движутся молекулы и тем выше давление газа.
Формула для вычисления давления идеального газа: PV = nRT, где P - давление, V - объем, n - количество вещества, R - газовая постоянная и T - температура. Эта формула называется уравнением состояния идеального газа.
Значение газовой постоянной зависит от единиц измерения. В системе SI (международная система единиц) значение газовой постоянной равно примерно 8.314 джоулей на моль·кельвин. В англо-американской системе единиц значение газовой постоянной равно примерно 0.0821 атм·л/моль·К.
Значение газовой постоянной в химии
В своей наиболее общей формулировке, газовая постоянная описывает пропорциональность между давлением (P), объемом (V) и температурой (T) идеального газа по формуле:
PV = nRT
где n - количество вещества газа, а T - абсолютная температура.
Значение газовой постоянной составляет приблизительно 8,314 Дж/(моль·К) или 0,0821 л·ат/(моль·К). Это значение может быть использовано для вычисления их различных параметров, таких как давление, объем или количество вещества, при данной температуре и давлении.
Использование газовой постоянной позволяет установить относительные числовые значения между этими различными параметрами и определить связь между ними. Также она играет важную роль в законе Гей-Люссака и законе Шарля, которые определяют поведение газов и их взаимосвязь при изменении объема и температуры.
Физическое определение газовой постоянной

Физически, газовая постоянная обозначается символом R и является универсальной для всех газов. Она представляет собой отношение между молярной массой газа (M) и его удельной газовой постоянной (Rн):
R = Rн/M
Здесь Rн - удельная газовая постоянная, которая выражается в Дж/(кг·К), а M - молярная масса газа, выражается в кг/моль.
Газовая постоянная также может быть выражена через универсальный газовый закон:
pV = nRT
Где p - давление газа, V - его объем, n - количество молей газа, T - абсолютная температура, а R - газовая постоянная.
Газовая постоянная имеет разные численные значения для разных единиц измерения (например, Дж/(моль·К), атм·л/(моль·К), Дж/(кг·К)), однако ее физическое значение остается неизменным и позволяет описывать свойства газов на молекулярном уровне.
Роль газовой постоянной в уравнении состояния идеального газа
Уравнение состояния идеального газа выглядит следующим образом:
pV = nRT
- p - давление газа
- V - объем газа
- n - количество вещества газа
- R - газовая постоянная
- T - температура газа
Газовая постоянная, обозначенная как R, зависит от единиц измерения давления, объема и температуры. Значение газовой постоянной может быть различным в разных системах единиц.
Использование газовой постоянной в уравнении состояния позволяет связать между собой физические характеристики газа и определить его состояние при известных параметрах. Уравнение состояния идеального газа является одним из основных законов физики и находит широкое применение в различных областях науки и техники.
Зависимость газовой постоянной от состояния вещества
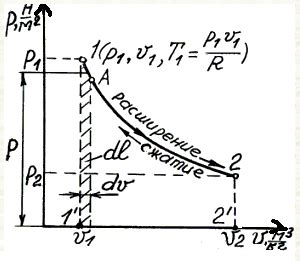
Однако, необходимо отметить, что газовая постоянная не является постоянной величиной и зависит от состояния вещества. Газовая постоянная R зависит от физических и химических свойств газа, таких как масса молекул, их движение, взаимодействие между молекулами и другие параметры.
Зависимость газовой постоянной от состояния вещества может быть выражена через уравнение состояния газа, которое учитывает влияние неидеальности газа и другие факторы. Например, для реальных газов существует уравнение вида: PV = ZnRT, где Z – коэффициент сжимаемости, который зависит от величины давления и температуры.
Таким образом, газовая постоянная является важным параметром, определяющим поведение газов при изменении давления, объема и температуры. Ее значение зависит от состояния вещества и может быть использовано для описания свойств различных газов и реакций, происходящих с их участием.
Величина газовой постоянной в различных единицах измерения
Значение газовой постоянной зависит от системы единиц измерения, в которой она выражается. В СИ (системе международных единиц) газовая постоянная имеет следующее значение:
| Единица измерения | Обозначение | Значение |
|---|---|---|
| Дж/моль·К | R | 8,314 |
Однако газовая постоянная может быть выражена и в других системах единиц. Например, в системе CGS (сантиметр-грамм-секунда) газовая постоянная имеет значение:
| Единица измерения | Обозначение | Значение |
|---|---|---|
| эрг/моль·К | R | 8,314×10^7 |
В этих двух системах единиц газовая постоянная имеет разные значения, однако она играет одну и ту же роль в описании свойств идеального газа и связанных с ним законов.
Применение газовой постоянной в химических расчетах

Газовая постоянная используется для описания зависимости между давлением, объемом, температурой и количеством вещества газа. Она является пропорциональной константой, которая связывает эти четыре параметра между собой посредством уравнения состояния идеального газа:
PV = nRT
где P - давление газа, V - его объем, n - количество вещества газа, T - температура в кельвинах, а R - газовая постоянная.
Значение газовой постоянной зависит от выбранной системы единиц. В международной системе единиц ее значение составляет примерно 8,314 дж/(моль·K), а в системе СГС - 82,057 см³·атм/(моль·K).
Применение газовой постоянной в расчетах позволяет определить различные характеристики газа, такие как его плотность, молярная масса, количество вещества и др. Она также помогает предсказывать поведение газовой смеси под различными условиями.
Значение газовой постоянной для нашей повседневной жизни
Газовая постоянная используется в различных научных и технических областях, включая физику, химию и инженерию. Она позволяет нам понять и описать, как газы ведут себя при различных условиях, таких как давление, объем и температура.
Значение газовой постоянной распространяется и на обычные ситуации из нашей повседневной жизни. Например, она помогает нам понять, как работает газовая плита или газовый котел. Газовая постоянная также важна для измерения и контроля газового потока, например, при использовании газовых счетчиков.
Кроме того, газовая постоянная используется для расчетов и моделирования различных технических процессов, таких как сжатие и расширение газа. Она помогает инженерам и ученым предсказывать и оптимизировать работу систем, связанных с газами, например, воздушных компрессоров, холодильных установок и систем отопления.
Таким образом, газовая постоянная играет важную роль в нашей повседневной жизни, позволяя нам лучше понять и управлять взаимодействием газов с окружающей средой и использовать эти знания в различных технических приложениях.








