Амфотерные металлы - это класс химических элементов, которые обладают свойствами как металлов, так и неметаллов. Такое уникальное поведение позволяет амфотерным металлам реагировать как с кислотами, так и с щелочами, в результате чего они могут образовывать разнообразные соединения.
Основные свойства амфотерных металлов связаны с их способностью изменять свой окислительно-восстановительный потенциал в зависимости от условий среды. Это значит, что амфотерные металлы могут терять или получать электроны, что делает их универсальными химическими агентами.
Примеры амфотерных металлов включают алюминий (Al), цинк (Zn), железо (Fe), свинец (Pb) и некоторые другие элементы. Например, алюминий образует соединения как с щелочами (например, NaOH), так и с кислотами (например, HCl), образуя соли и водород. Это свойство амфотерных металлов обусловлено особенностями их электронной структуры и связи между атомами.
Изучение амфотерных металлов имеет большое значение для различных областей науки и техники, включая химию, материаловедение и электрохимию. Понимание их основных свойств помогает улучшить синтез и свойства материалов, разрабатывать новые эффективные катализаторы и улучшать процессы электрохимической преобразования энергии.
Амфотерные металлы: основные свойства и примеры
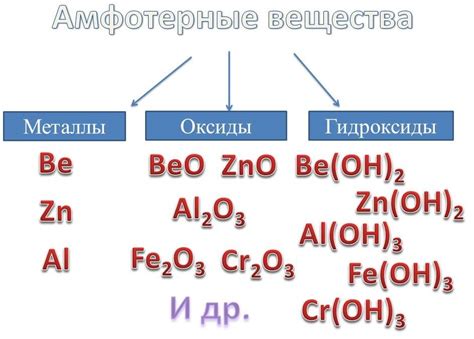
Один из основных признаков амфотерных металлов - способность образовывать амфотерные оксиды, т.е. вещества, которые могут растворяться как в кислотной среде, так и в щелочной. Это свойство позволяет амфотерным металлам образовывать различные соли и соединения с разными химическими и физическими свойствами.
Примерами амфотерных металлов являются алюминий (Al), цинк (Zn), железо (Fe), свинец (Pb) и некоторые другие элементы. Например, оксид алюминия (Al2O3) является амфотерным оксидом и может растворяться как в кислотах, так и в щелочах. Также, соли амфотерных металлов, например алюминий сульфат (Al2(SO4)3), могут проявлять как кислотные, так и основные свойства.
Амфотерные металлы имеют широкий спектр применений и используются в различных отраслях промышленности, а также в научных исследованиях. Они также играют важную роль в живых организмах и находятся в составе многих биологически активных веществ.
Что такое амфотерные металлы?
Основными свойствами амфотерных металлов являются:
- Реактивность со средами разного характера. Амфотерные металлы могут взаимодействовать не только с кислотами, но и с основаниями. Кислотно-основная реакция протекает в результате передачи протона из одной молекулы в другую.
- Способность образовывать соли. Амфотерные металлы могут образовывать соли как с кислотами, так и с основаниями. Это обусловлено их способностью взаимодействовать с различными веществами и образовывать разнообразные соединения.
- Изменяемость окисления и восстановления. Амфотерные металлы могут изменять свою степень окисления в ходе химических реакций. Они могут как окисляться, так и восстанавливаться.
Некоторые примеры амфотерных металлов включают алюминий (Al), железо (Fe), цинк (Zn), олово (Sn) и свинец (Pb). Эти металлы имеют широкий спектр применения и используются в различных отраслях промышленности, включая производство легких сплавов, строительство, производство электроники и др.
Основные свойства амфотерных металлов

Основные свойства амфотерных металлов включают:
- Реактивность. Амфотерные металлы могут проявлять реактивность как с кислотными, так и с щелочными веществами. Они могут расстворяться в кислотах и основаниях, а также взаимодействовать с ними, образуя соли и воду.
- Ионизация. Амфотерные металлы способны образовывать положительно заряженные ионы (катионы) и отрицательно заряженные ионы (анионы) в растворе. Это позволяет им участвовать в различных химических реакциях и образовывать стабильные соединения.
- Восстановительные свойства. Амфотерные металлы могут проявлять восстановительные свойства и участвовать в реакциях, в которых переходят из более низкого окисления в более высокое состояние окисления.
- Способность образовывать амфотерные оксиды. Амфотерные металлы образуют оксиды, которые могут образовывать как кислотные, так и основные растворы взаимодействуя с водой. Это связано с реакцией металлического оксида с водой, в результате которой образуются ионы гидроксида или ионы водорода.
Примеры амфотерных металлов включают алюминий (Al), цинк (Zn), свинец (Pb), железо (Fe). Эти металлы имеют широкий спектр применений в различных областях, включая строительство, электронику, медицину и другие.
Примеры амфотерных металлов
Примерами амфотерных металлов являются алюминий (Al), цинк (Zn) и свинец (Pb).
Алюминий является одним из самых распространенных амфотерных металлов. Он может реагировать с кислотами, вытесняя водород и образуя соли. Также алюминий способен реагировать с основаниями, образуя алюминаты.
Цинк также проявляет амфотерные свойства. Он может реагировать с кислотами, вытесняя водород и образуя соли, а также реагировать с основаниями и образовывать цинкаты.
Свинец является амфотерным металлом, способным реагировать как с кислотами, так и с основаниями. Это свойство свинца используется в различных промышленных процессах и в производстве различных соединений.
Реакции амфотерных металлов
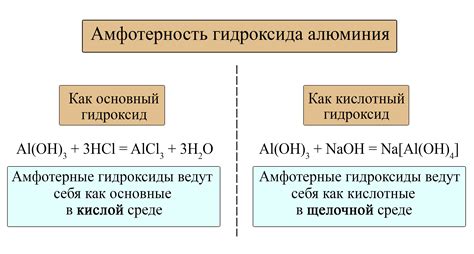
Когда амфотерные металлы взаимодействуют с кислотами, они образуют соли. Например, алюминий (Al) может реагировать с соляной кислотой (HCl) и образовывать соль алюминия - хлорид алюминия (AlCl3).
С другой стороны, амфотерные металлы также могут реагировать с щелочами и образовывать гидроксиды. Например, оксид алюминия (Al2O3) реагирует с натриевой гидроксидной (NaOH) щелочью, образуя гидроксид алюминия - Al(OH)3.
Реакции амфотерных металлов происходят благодаря специфической структуре и электронной конфигурации этих металлов. У них присутствуют свободные электроны, которые могут участвовать в химических реакциях.
Примеры амфотерных металлов:
- Алюминий (Al)
- Залежи товарного свинца (PbO)
- Цинк (Zn)
- Титан (Ti)
- Тин (Sn)
Таким образом, амфотерные металлы обладают уникальными свойствами, позволяющими им реагировать как с кислотами, так и с щелочами, что делает их важными и широко используемыми в химии и промышленности.
Использование амфотерных металлов
- Электрохимия: амфотерные металлы, такие как железо, алюминий и цинк, используются для производства гальванических элементов и батарей.
- Металлургия: алюминий и цинк находят широкое применение при производстве различных сплавов. Они используются в авиационной и автомобильной промышленности, а также в производстве строительных материалов.
- Химическая промышленность: амфотерные металлы являются важными катализаторами во многих химических реакциях. Они применяются в производстве пластмасс, красителей, лекарственных веществ и других химических продуктов.
- Электроника: многие амфотерные металлы, включая кремний и германий, используются в производстве полупроводников и электронных приборов.
- Медицина: амфотерные металлы могут использоваться в медицинских приборах и имплантатах благодаря их биологической совместимости.
Использование амфотерных металлов в различных областях продолжает развиваться, и их роль в современных технологиях становится все более значимой.








