Валентность — это химический параметр, отражающий способность атомов элементов образовывать химические связи. Кислород, один из наиболее распространенных элементов в природе, имеет валентность равную 2. Это значит, что каждый атом кислорода способен образовывать две химические связи с другими атомами.
Валентность кислорода влияет на его химические свойства и реакционную способность. Именно благодаря своей валентности равной 2, кислород может быть активным в многих сильно окисляющих реакциях. Он легко образует соединения с другими элементами, такими как водород, углерод, азот и многими другими, образуя различные оксиды, карбонаты, серы и другие соединения.
Кислород — один из ключевых компонентов воздуха и находится во многих органических и неорганических веществах. Его валентность равная 2 делает его важным участником многих химических процессов, включая дыхание организмов, горение и разложение веществ.
Знание валентности кислорода помогает химикам понять, как он будет взаимодействовать с другими элементами и какие соединения можно с ним образовать. Изучение валентности кислорода имеет огромное значение в химии, медицине, окружающей среде и других областях науки.
Валентность кислорода и ее значение
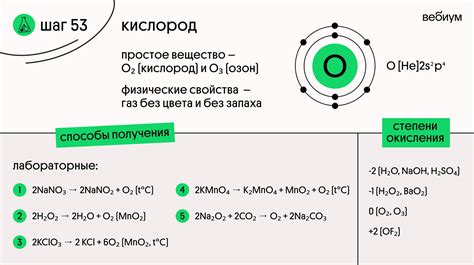
У кислорода валентность равна 2, что означает, что атом кислорода в спокойном состоянии имеет 6 валентных электронов в своей внешней оболочке. Кислород стремится заполнить свою внешнюю оболочку в восемь электронов, чтобы достичь стабильной октетной конфигурации.
Это свойство делает кислород активным элементом, который может образовывать химические связи с другими элементами и образовывать различные соединения. Кислород способен образовывать до двух связей с другими атомами, включая другие атомы кислорода.
Важность валентности кислорода заключается в его способности участвовать во многих химических реакциях и образовывать разнообразные химические соединения. Оксиды, кислородные кислоты, соли кислот и многие другие соединения с кислородом являются важными основами химии и играют важную роль в различных процессах природы и промышленности.
Таким образом, валентность кислорода равна 2 и она играет ключевую роль в его способности образовывать соединения и участвовать в химических реакциях.
Что такое валентность?
Конкретное значение валентности атома зависит от его расположения в таблице Менделеева и количества электронов на его валентной оболочке. Например, для атома кислорода его валентность равна 2, что значит, что он имеет потенциал принять 2 электрона от другого атома или образовать две химические связи.
Знание валентности атома позволяет предсказывать его химическую активность и типы связей, которые он может образовывать. Валентность является основным понятием в химии и используется для определения структуры и свойств химических соединений.
Как определяется валентность кислорода?
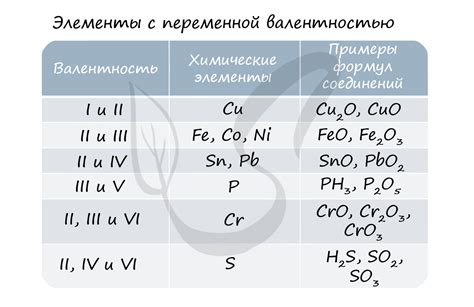
Валентность кислорода может изменяться в некоторых случаях. Например, в некоторых соединениях, кислород может образовывать одну связь и иметь валентность 1. Также, кислород может образовывать тройные связи и иметь валентность 3.
Определение валентности кислорода имеет важное значение в химических реакциях и свойствах соединений. Зная валентность кислорода, мы можем определить молекулярную форму соединения и предсказать его реакционную способность.
Роль валентности кислорода в химических реакциях
Валентность кислорода имеет важное значение в химических реакциях и играет роль во многих процессах:
- Образование оксидов: Кислород может образовывать соединения с другими элементами, образуя оксиды. Валентность 2 позволяет кислороду образовывать две связи и стабилизироваться в оксидных формах, таких как оксид углерода (CO2) или оксид серы (SO2).
- Окислительные реакции: Валентность кислорода определяет его способность выступать в реакциях окисления. Кислород с валентностью 2 может принимать электроны от других веществ, окисляясь при этом. Это позволяет кислороду выступать в качестве сильного окислителя и участвовать в многих окислительно-восстановительных реакциях.
- Ацидное поведение: За счет высокой электроотрицательности атома кислорода и его валентности 2, кислород может образовывать кислоты и проявлять ацидные свойства. Кислородные кислоты, такие как серная кислота (H2SO4) или азотная кислота (HNO3), являются важными химическими соединениями и активно участвуют в химических реакциях.
Валентность кислорода играет ключевую роль во множестве химических реакций и процессов, определяя его возможности в образовании связей, окислительных свойствах и ацидном поведении. Это позволяет кислороду участвовать в формировании разнообразных химических соединений и реакциях, важных для жизни и функционирования различных организмов.
Как валентность влияет на свойства веществ?
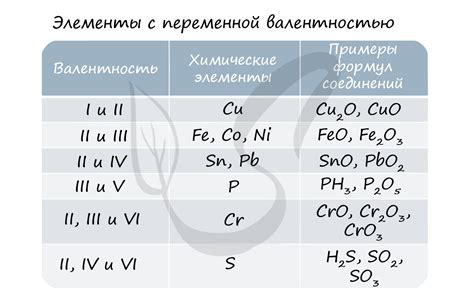
Валентность кислорода равна 2, что означает, что он способен образовывать связи с двумя другими элементами. Кислород является очень активным элементом, и его валентность сильно влияет на свойства веществ, в которых он участвует.
Кислород образует соединения с различными элементами, включая металлы и неметаллы. Он может образовывать ковалентные связи с другими неметаллами, такими как углерод и сера. Ковалентные соединения кислорода обладают обычно высокой температурой плавления и кипения, а также хорошей растворимостью в воде.
Кислород также может образовывать ионные соединения с металлами, например, оксиды. В ионных соединениях кислорода оказывается отрицательно заряженным. Ионные соединения, в которых участвует кислород, обычно обладают высокой теплопроводностью и электропроводностью.
Валентность кислорода 2 позволяет ему образовывать гидроксиды и пероксиды. Гидроксиды кислорода являются щелочными соединениями, а пероксиды обладают окислительными свойствами.
Таким образом, валентность кислорода влияет на его способность образовывать различные типы связей и соединений. Это делает его одним из самых важных и широко распространенных элементов в химии и природе в целом.
Примеры соединений с валентным кислородом
Вот некоторые примеры соединений, в которых присутствует валентный кислород:
- Вода (H2O) - одна из самых известных соединений с кислородом. Здесь два атома водорода связаны с атомом кислорода.
- Серная кислота (H2SO4) - вещество, широко использующееся в промышленности. Оно содержит два атома водорода, один атом серы и четыре атома кислорода.
- Диоксид углерода (CO2) - газ, вызывающий парниковый эффект. В нем два атома кислорода связаны с одним атомом углерода.
- Азотная кислота (HNO3) - кислотное соединение, используемое в химической промышленности. Оно содержит атомы водорода, азота и кислорода.
Это лишь некоторые примеры соединений с валентным кислородом. Кислород является важным элементом во многих органических и неорганических соединениях, и его валентность 2 позволяет ему образовывать различные химические связи, что делает его основным компонентом множества веществ.
Значение валентности кислорода для биологических процессов
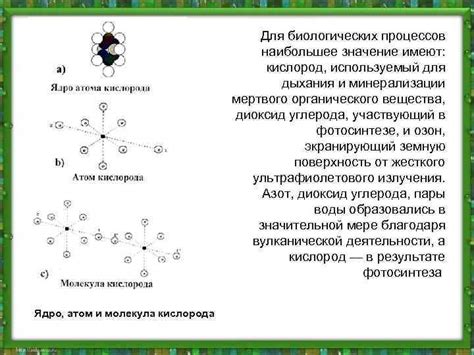
Валентность кислорода равна 2, что в контексте биологических процессов имеет большое значение. Кислород играет важную роль в организмах, таких как животные и растения.
Кислород необходим для клеточного дыхания, процесса, при котором клетки получают энергию из пищи. Валентность 2 у кислорода позволяет ему образовывать две ковалентные связи с другими атомами, что делает его одним из самых электроотрицательных элементов и способствует его включению в различные сложные структуры молекул.
Одним из основных примеров включения кислорода в биологические процессы является процесс окисления. Кислород участвует в окислительных реакциях, в результате которых энергия освобождается для использования клеткой.
Также, кислород играет важную роль в метаболизме жиров и углеводов, процессе, в результате которого клетки расщепляют энергию, хранящуюся в молекулах пищи. Благодаря валентности 2, кислород образует ковалентные связи с атомами углерода и водорода, образуя такие важные молекулы, как углеводы и жиры.
Кроме того, кислород играет ключевую роль в процессе фотосинтеза у растений. Валентность 2 позволяет кислороду образовывать связи с другими элементами, такими как углерод, и создавать сложные органические молекулы, такие как глюкоза.
В заключение, валентность кислорода равная 2 отражает его способность образовывать ковалентные связи с другими атомами, что важно для осуществления биологических процессов, таких как клеточное дыхание, окисление, метаболизм и фотосинтез.
Валентность кислорода в атмосфере и экологические последствия
Валентность кислорода играет важную роль в химических реакциях и взаимодействии с другими элементами. Например, кислород может образовывать соединения с другими элементами, такими как углерод, водород, азот и многими другими. При этом кислород может выступать в качестве электронного донора или акцептора, что является основой многих биологических процессов.
Однако, нарушение баланса содержания кислорода в атмосфере может иметь серьезные экологические последствия. Например, увеличение содержания кислорода в атмосфере может привести к повышению температуры и изменению климата планеты. Кроме того, резкое изменение валентности кислорода может вызвать разрушение экологических систем и угрозу жизни на Земле.
Итак, понимание валентности кислорода является важным для понимания не только химических процессов, но и экологической ситуации на планете. Учет этого фактора в масштабе планеты позволяет более глубоко и точно анализировать и предсказывать изменения, происходящие в окружающей среде.
| Примеры соединений с кислородом | Валентность кислорода |
|---|---|
| Углекислый газ (CO2) | 4 |
| Вода (H2O) | 2 |
| Озон (O3) | 3 |
Способы использования валентного кислорода в промышленности

Валентность кислорода, равная 2, делает его особенно полезным и востребованным в промышленности. Ниже представлены некоторые из способов использования валентного кислорода:
- Процесс окисления: Валентный кислород может быть использован в промышленных процессах для окисления различных веществ. Это позволяет получить окисленные продукты с измененными свойствами, например, окисление металлов для создания окисных пленок, или окисление органических соединений для получения новых продуктов.
- Очистка воды и сточных вод: Валентный кислород также может использоваться для очистки воды и сточных вод. Он применяется в процессах окисления и разложения различных загрязняющих веществ, таких как органические соединения и металлы. Этот процесс помогает улучшить качество воды и снизить загрязнение окружающей среды.
- Производство химических соединений: Валентный кислород является необходимым компонентом в процессе производства многих химических соединений. Например, он используется в производстве пероксидов, карбоксиловых кислот и азотных соединений. Валентный кислород участвует в химических реакциях, обеспечивая нужную степень окисления соединений.
- Медицинские приложения: Валентный кислород также находит применение в медицинской промышленности. Он используется в кислородной терапии для лечения дыхательных заболеваний и дыхательной недостаточности. Валентный кислород поставляется пациентам через специальные приборы, такие как кислородные маски или кислородные баллоны.
- Процессы сгорания: Валентный кислород может быть использован в процессах сгорания для увеличения эффективности и мощности. Он используется в ракетных двигателях, некоторых видов двигателей внутреннего сгорания и других технологиях, где требуется высокая энергетическая мощность.
Валентный кислород со своей валентностью 2 имеет широкий спектр применений в промышленности и оказывает значительное влияние на многие процессы и технологии. Благодаря своим уникальным свойствам, он является одним из наиболее востребованных веществ в промышленности и научных исследованиях.








